Có 100 ml dung dịch X gồm NH4+, K+, CO32- ; SO42-. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 2,24 lít (đktc) khí NH3 và 66,3 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Tính giá trị của m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
+ Bản chất phản ứng: P 2 : 2 H + + C O 3 2 - H 2 O + C O 2 ↑ ⇒ n C O 3 2 - = n C O 2 = 0 , 1 P 1 : N H 4 + + O H - N H 3 ↑ + H 2 O B a 2 + + C O 3 2 - B a C O 3 ↓ B a 2 + + S O 4 2 - B a S O 4 ↓ ⇒ n N H 4 + = n N H 3 = 0 , 3 n B a C O 3 = n C O 3 2 - = 0 , 1 n B a S O 4 = ( 43 - 0 , 1 . 197 ) : 233 = 0 , 1 + B T Đ T t r o n g m ộ t n ử a X : n K + = 2 n S O 4 2 - + 2 n C O 3 2 - - n N H 4 + = 0 , 1 m m u ố i t r o n g X = 2 ( m N H 4 + + m K + + m S O 4 2 - + m C O 3 2 - ) = 49 , 8 g a m

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

Chọn đáp án A
Chú ý tỉ lệ dung dich X trong mỗi phản ứng
Gọi số mol ion Na+, NH4+, CO32- và SO42- trong 100ml lần lượt a, b, c, d mol
Khi cho X tác dụng với HCl chỉ có CO32- tham gia phản ứng → c = 0,1 mol
Khi cho X tác dụng với BaCl2 thu được BaCO3 và BaSO4 → 0,1.197 + d.233= 43 → d = 0,1 mol
Khi cho X tác dụng lượng dư dung dịch NaOH chỉ có NH4+ tham gia phản ứng → b = 0,2 mol
Bảo toàn điện tích trong dung dịch X → a = 2. 0,1 + 2. 0,1 -0,2 = 0,2 mol
Vậy trong 300ml dung dịch X gồm 0,6 mol Na+, 0,6 mol NH4+, 0,3 mol CO32- và 0,3 mol SO42-
→ m = 0,6.23 + 0,6. 18 + 0,3. 60 + 0,3. 96= 71,4 gam.
Đáp án A.

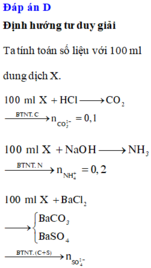
Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
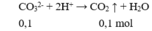
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
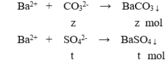
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
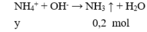
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.

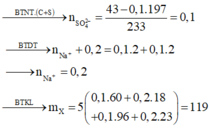


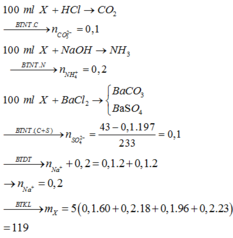
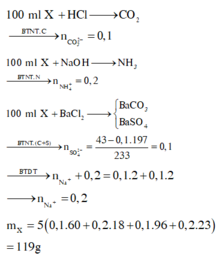

- Phần 1:
\(n_{NH_4^+}=n_{NH_3}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(197n_{CO_3^{2-}}+233n_{SO_4^{2-}}=66,3\left(1\right)\)
- Phần 2:
\(n_{CO_3^{2-}}=n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Thay vào (1) ⇒ nSO42- = 0,2 (mol)
BT điện tích trong 50ml dd, có: nNH4+ + nK+ = 2nCO32- + 2nSO42-
⇒ mK+ = 2.0,1 + 2.0,2 - 0,1 = 0,5 (mol)
⇒ m = 2.(0,1.18 + 0,1.60 + 0,2.96 + 0,5.39) = 93 (g)