Để 2 cốc đựng dd \(H_2SO_4\) (cốc 1) và dd \(HCl\) (cốc 2) trên hai dĩa cân sao cho ở vị trí cân bằng. Sau đó, cùng lúc cho vào cốc (1) 20g Zn và cốc (2) 20g Al. Hãy cho biết sau khi hai cốc xảy ra phản ứng hoàn toàn, cân còn ở vị trí cân bằng nữa không? Nếu không, cân lệch về phía nào? Giải thích?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Xét cốc đựng HCl
\(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15-------------------->0,15
=> \(m_{tăng}=8,4-0,15.2=8,1\left(g\right)\) (1)
- Xét cốc đựng H2SO4:
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}\)---------------------------->\(\dfrac{m}{18}\)
=> \(m_{tăng}=m-\dfrac{m}{18}.2=\dfrac{8}{9}m\left(g\right)\) (2)
(1)(2) => \(\dfrac{8}{9}m=8,1\) => 9,1125 (g)

nCaCO3 = 20/100 = 0.2 (mol)
CaCO3 + 2HCl => CaCl2 + CO2 + H2O (1)
0.2_____________________0.2
2Al + 3H2SO4 => Al2(SO4)3 + 3H2 (2)
a_________________________1.5a
Vì cân bằng nên :
m bình (1) tăng = m bình (2) tăng
=> mCaCO3 - mCO2 = mAl - mH2
=> 20 - 0.2*44 = 27a - 1.5a*2
=> a = 7/15
mAl = 7/15 * 27= 12.6 (g)

cốc A: Fe + 2HCl -> FeCl2 + H2 (H2 bay hơi) (1)
0,2 0,2 0,2
cốc B: 2Al +3H2SO4 -> Al2(SO4)3 + 3H2 (H2 bay hơi) (2)
a \(\frac{3a}{2}\)
gọi a số mol Al
khi Fe và Al hòa tan hết khuấy đều hòa tan hết thấy còn ở vị trí cân bằng tức là khối lượng 2 bình bằng nhau
cốc A: thêm Fe, giải phóng H2
cốc B: thêm Al, giải phóng H2
<=> \(m_{Fe}-m_{H_2\left(1\right)}=m_{Al}+m_{H_2\left(2\right)}\)
\(\Leftrightarrow11,2-0,2\cdot2=27a-\frac{3}{2}a\cdot2\)
\(\Leftrightarrow a=0,45\Leftrightarrow m=0,45\cdot27=12,15\left(g\right)\)
vậy m=12,15(g)

Đáp án C
Dễ dàng nhận thấy CaCO3 và KHCO3 có cùng phân tử khối, cùng số mol và khi phản ứng với dung dịch HCl thì thoát ra lượng CO2 như nhau.

\(n_{Mg}=\dfrac{13.44}{24}=0.56\left(mol\right)\)
TN1 :
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.56................................0.56\)
TN2 :
\(MCO_3+H_2SO_4\rightarrow MSO_4+CO_2+H_2O\)
\(x............................x\)
Vì cân thăng bằng nên :
\(m_{Mg}-m_{H_2}=m_{MCO_3}-m_{CO_2}\)
\(\Rightarrow13.44-0.56\cdot2=22-44x\)
\(\Rightarrow x=0.22\)
\(M_{MCO_3}=\dfrac{22}{0.22}=100\left(g\text{/}mol\right)\)
\(\Rightarrow M=100-60=40\left(g\text{/}mol\right)\)
\(M:Ca\)

$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
$n_{BaSO_4} = n_{Na_2SO_4} = \dfrac{10}{142}(mol)$
$m_{BaSO_4} = \dfrac{10}{142}.233 = 16,4(gam)$
$AgNO_3 + NaCl \to AgCl + NaNO_3$
$n_{AgCl} = n_{NaCl} = \dfrac{10}{58,5}(mol)$
$m_{AgCl} = \dfrac{10}{58,5}.143,5 = 24,53(gam)$
Do đó cân lệnh về vị trí bên phải

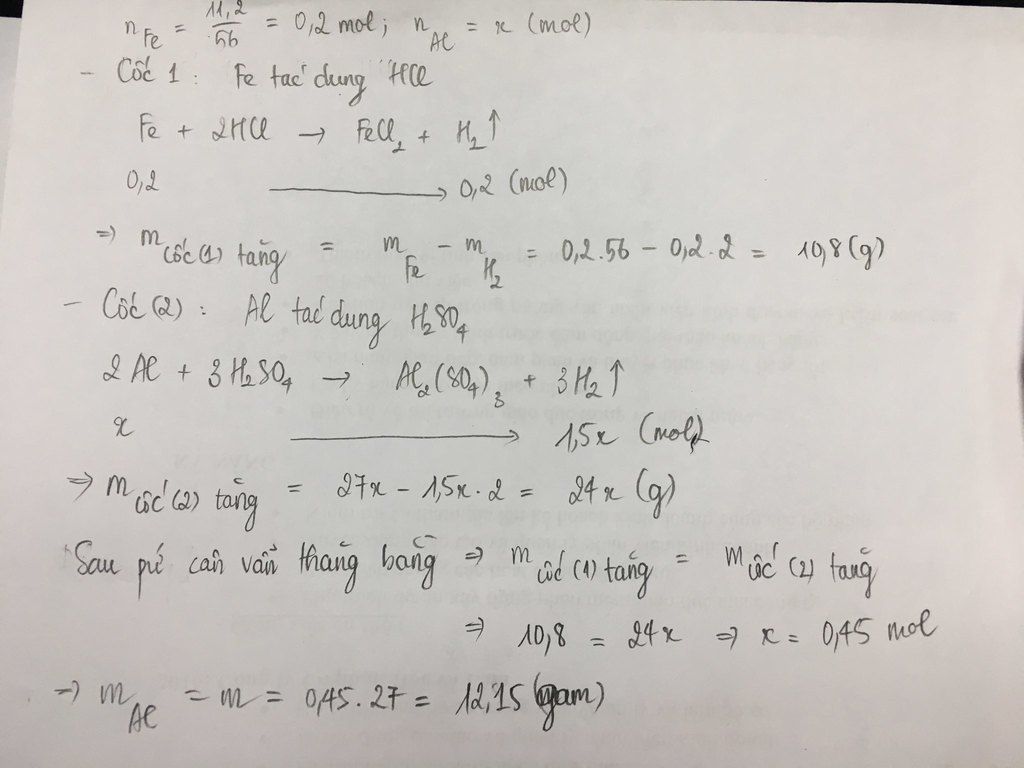
\(n_{Zn}=\dfrac{m}{M}=\dfrac{20}{65}\approx0,3\left(mol\right)\)
\(n_{Al}=\dfrac{m}{M}=\dfrac{20}{27}\approx0,7\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\left(1\right)\)
TĐB: 0,3 0,3 0,3 (mol)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\left(2\right)\)
TĐB: 0,7 2,1 1,05 (mol)
Tỉ lệ \(n_{H_{2\left(1\right)}}\) thoát ra ít hơn tỉ lệ \(n_{H_{2\left(2\right)}}\)
\(\Rightarrow\) Cân lệch về phía cốc 2