Cho 20g hỗn hợp X gồm CuO và Fe2O3 tác dụng vừa đủ với 0,2l dung dịch HCl 3,5M. Tính thành phần phần trăm khối lượng của mỗi oxit ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn B
Gọi a là số mol của CuO và b là số mol của F e 2 O 3 có trong 20 gam
hh 200 ml dd HCl 3,5 M => nHCl = 0,2 . 3,5 = 0,7 mol
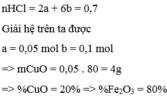

Gọi a,b là số mol của CuO và Fe2O3
Ta có pương trình 80a+160b=20(1)
Ta có các phương trình sau
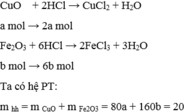
CuO + 2 HCl ➞ CuCl2 +H2
a..............2a............a.........a........(mol)
Fe2O3 + 6 HCl ➞ 2 FeCl3 + 3H2O
b.................6b.............2b..........3b........(mol)
Ta có\(\sum\limits\)nHCl=2a+6b=0.2*3.5=0.7(mol) (2)
Giải (1) và (2) ta được a=0.05;b=0.1
%Fe=((0.1*64)/20)*100%=32%
%Cu=100%-32%=68%

\(n_{HCl}=0,5.1=0,5\left(mol\right)\)
a)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x------->2x
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
y--------->6y
Có hệ: \(\left\{{}\begin{matrix}2x+6y=0,5\\80x+160y=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
\(m_{CuO}=0,1.80=8\left(g\right)\\ m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
b
\(\%m_{CuO}=\dfrac{0,1.80.100\%}{16}=50\%\\ \%m_{Fe_2O_3}=\dfrac{0,05.160.100\%}{16}=50\%\)

CuO+2HCl--->CuCl2+H2O
x 2x x x
Fe2O3+6HCl--->2FeCl3+3H2O
y 6y 2y 3y
nHCl=3,5.0,2=0,7 mol
gọi x y lần lượt là nCuO,nFe2O3
ta có x.80+y.160=20
2x+6y=0,7 giải hệ pt ta có x=0,05 y=0,1
mCuO=0,05.80=4g
mFe2O3=0,1.160=16g
%mCuO=4/20 .100%=20%
%mFe2O3=100%-20%=80%

\(n_{HCl}=3.0,2=0,6(mol)\\ PTHH:Fe_2O_3+6HCl\to 2FeCl_3+3H_2O\\ \Rightarrow n_{Fe_2O_3}=\dfrac{1}{6}n_{HCl}=0,1(mol)\\ \Rightarrow m_{Fe_2O_3}=0,1.160=16(g)\\ \Rightarrow \%_{Fe_2O_3}=\dfrac{16}{20}.100\%=80\%\\ \Rightarrow \%_{Cu}=100\%-80\%=20\%\)

Gọi x,y là số mol của CuO,Fe2O3
Ta có: 80x+160y=20 (1)
nHCl= 3,5.0.,2 = 0,7
PTHH:2HCl + CuO → CuCl2 + H2O
Mol: 2x x
PTHH:6HCl + Fe2O3 → 2FeCl3 + 3H2O
Mol: 6y y
⇒ 2x+6y=0,7 (2)
Từ (1)(2)⇒ x=0,05;y=0,1
\(\Rightarrow m_{CuO}=0,05.80=4\left(g\right);m_{Fe_2O_3}=0,1.160=16\left(g\right)\)

a) Gọi số mol Mg, CuO là a, b (mol)
=> 24a + 80b = 14 (1)
\(n_{HCl}=\dfrac{255,5.10\%}{36,5}=0,7\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a--->2a--------->a------>a
CuO + 2HCl --> CuCl2 + H2O
b------>2b----->b
=> 2a + 2b = 0,7 (2)
(1)(2) => a = 0,25 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,25.24}{14}.100\%=42,857\%\\\%m_{CuO}=\dfrac{0,1.80}{14}.100\%=57,143\%\end{matrix}\right.\)
b)
mdd sau pư = 14 + 255,5 - 0,25.2 = 269 (g)
\(C\%_{MgCl_2}=\dfrac{0,25.95}{269}.100\%=8,829\%\)
\(C\%_{CuCl_2}=\dfrac{0,1.135}{269}.100\%=5,019\%\)
\(n_{HCl}=0,2.3,5=0,7\left(mol\right)\\ n_{CuO}=a;n_{Fe_2O_3}=b\\ CuO+2HCl\xrightarrow[]{}\Rightarrow CuCl_2+H_2O\\ Fe_2O_3+6HCl\xrightarrow[]{}2FeCl_3+H_2O\\ \left\{{}\begin{matrix}2a+6b=0,7\\80a+160b=20\end{matrix}\right.\\\Rightarrow a=0,05;b=0,1\\ \%_{CuO}=\dfrac{0,05.80}{20}\cdot100=20\%\\ \%_{Fe_2O_3}=\dfrac{0,1.160}{20}\cdot100=80\%\)