Cho 12,4 g Na2O tác dụng với 0,3 mol H2O kết thúc phản ứng thu được NaOH.Hỏi chất nào dư và dư bao nhiêu gam?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


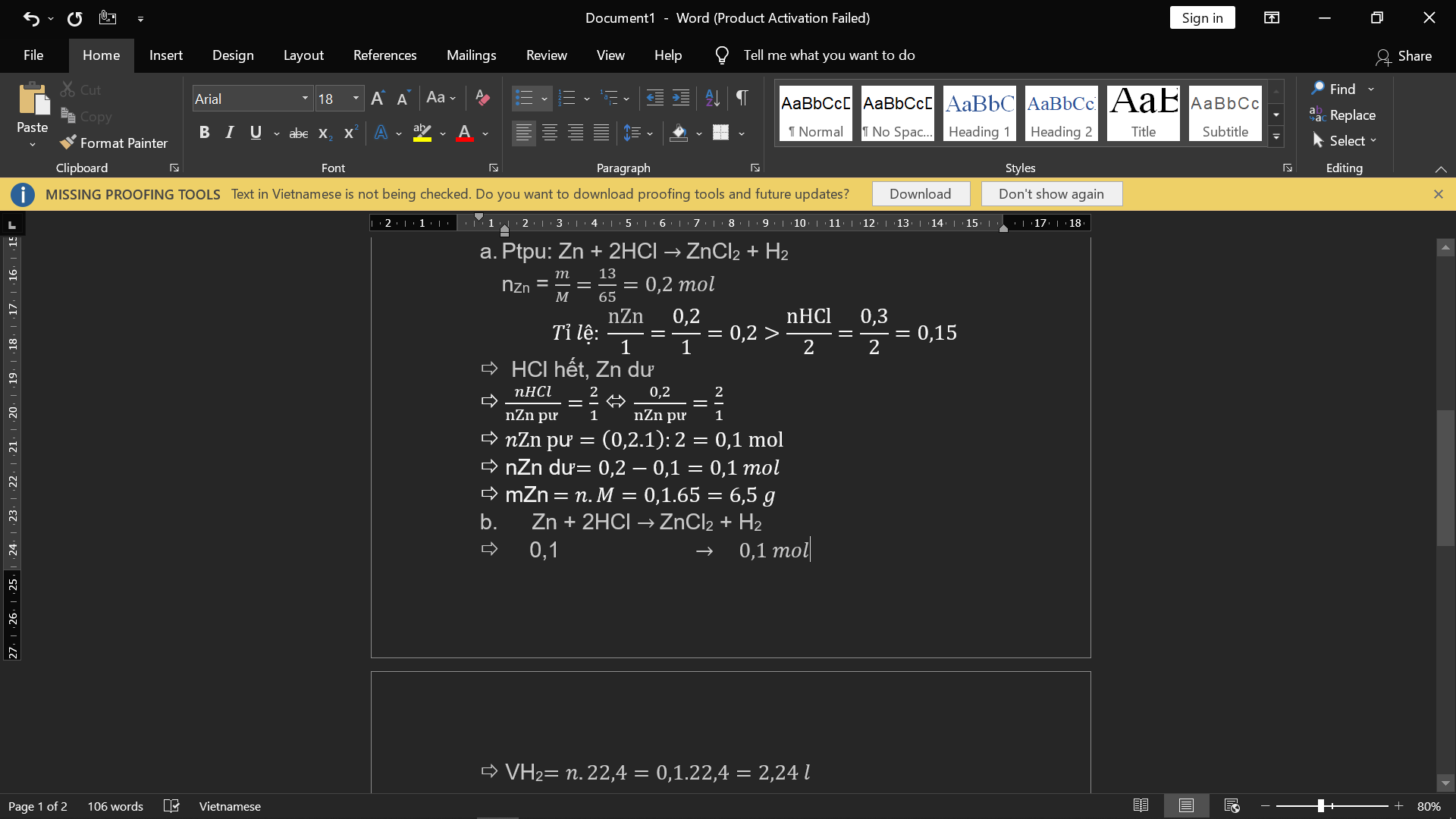
\(a) Zn + 2HCl \to ZnCl_2 + H_2\\ n_{Zn} = \dfrac{13}{65} = 0,2(mol)\\ \dfrac{n_{Zn}}{1} = 0,2 > \dfrac{n_{HCl}}{2} = 0,15 \to Zn\ dư\\ n_{Zn\ pư} = \dfrac{1}{2}n_{HCl} = 0,15(mol)\\ m_{Zn\ dư} = (0,2 - 0,15).65 = 3,25(gam)\\ b) n_{H_2} = n_{Zn\ pư} = 0,15(mol) \Rightarrow V_{H_2} = 0,15.22,4 = 3,36(lít)\)

Bài 1:
a) nP=6,2/31=0,2(mol); nO2= 6,72/22,4=0,3(mol)
PTHH: 4P + 5 O2 -to-> 2 P2O5
Ta có: 0,2/4 < 0,3/5
=> P hết, O2 dư, tính theo nP
=> nO2(p.ứ)= 5/4. nP= 5/4. 0,2=0,25(mol)
=> mO2(dư)=0,3- 0,25=0,05(mol)
=> mO2(dư)=0,05.32=1,6(g)
b) nP2O5= nP/2= 0,2/2=0,1(mol)
=>mP2O5=0,1.142=14,2(g)

Ta có: \(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Gọi: nNa = nBa = a (mol)
BT e, có: \(a+2a=0,06.2\Rightarrow a=0,04\left(mol\right)\)
Có: \(n_{OH^-}=2n_{H_2}=0,12\left(mol\right)\)
\(Al_2O_3+2OH^-\rightarrow2AlO_2^-+H_2O\)
\(n_{Al_2O_3\left(pư\right)}=\dfrac{1}{2}n_{OH^-}=0,06\left(mol\right)\)
0,2m gam chất rắn không tan là Al2O3
⇒ m chất rắn tan = 0,8m (g) = mNa + mBa + mAl2O3 pư = 12,52 (g)
\(\Rightarrow m=\dfrac{12,52}{0,8}=15,65\left(g\right)\)

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{Zn}=\dfrac{13}{65}=0,2(mol)\)
Vì \(\dfrac{n_{Zn}}{1}>\dfrac{n_{HCl}}{2}\) nên Zn dư
\(\Rightarrow n_{Zn({\text{phản ứng})}}=\dfrac{1}{2}n_{HCl}=0,15(mol)\\ \Rightarrow n_{Zn(\text{dư})}=0,2-0,15=0,05(mol)\\ \Rightarrow m_{Zn(\text{dư})}=0,05.65=3,25(g)\\ c,n_{ZnCl_2}=n_{H_2}=\dfrac{1}{2}n_{HCl}=0,15(mol)\\ \Rightarrow a=m_{ZnCl_2}=0,15.136=20,4(g)\\ V=V_{H_2}=0,15.22,4=3,36(l)\)

PT: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,25}{1}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{1}{2}n_{Mg}=0,1\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,1=0,15\left(mol\right)\)
Bạn tham khảo nhé!
PTHH: \(2Mg+O_2\underrightarrow{t^o}2MgO\)
Ta có: \(\left\{{}\begin{matrix}n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\n_{O_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,25}{1}\) \(\Rightarrow\) Magie p/ứ hết, Oxi còn dư
\(\Rightarrow n_{O_2\left(dư\right)}=0,25-0,1=0,15\left(mol\right)\)

Đáp án A
a mol HCHO phản ứng tráng bạc thu được X gam Ag => x = 4a.108(g)
Oxi hóa a mol HCHO với hiệu suất 50% sẽ thu được hỗn hợp B gồm 0,5 a mol HCOOH và 0,5a mol HCHO dư
Vì HCOOH cũng tham gia phản ứng tráng bạc
=> nAg = 4nHCHO dư + 2nHCOOH
=>y = 108. (4.0,5a+2.0,5a) = 108.3a (g)
Vậy y x = 3 4
\(n_{Na2O}=\dfrac{12,4}{62}=0,2\left(mol\right)\)
Pt : \(Na_2O+H_2O\rightarrow2NaOH\)
0,2 0,3
Xét tỉ lệ : \(\dfrac{0,2}{1}< \dfrac{0,3}{1}=>\) H2O dư
\(n_{H2O\left(dư\right)}=0,3-0,2=0,1\left(mol\right)\)
⇒ \(m_{H2O\left(dư\right)}=0,1.18=1,8\left(g\right)\)
Chúc bạn học tốt