đốt cháy hoàn toàn m gam hợp chất a (chỉ chứa các nguyên tố c.hn) bằng lượng không khí vừa thu được 17,6 gam co2 ; 12,6 gam h2o ;69,44lít n2 (đktc)xác định công thứ hoá học của a biết trong không khí n2 chiếm 80% thể tích khối lượng mol của A là 45
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn C: nC = 0,4 (mol) => mC = 0,4.12 = 4,8(g)
\(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
Bảo toàn H: nH = 0,9 (mol) => mH = 0,9.1 = 0,9 (g)
\(n_{N_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Bảo toàn N: nN = 0,1 (mol) => mN = 0,1.14 = 1,4 (g)

n C = n C O 2 = 17 , 6 44 = 0 , 4 m o l ; n H = 2. n H 2 O = 2. 12 , 6 18 = 1 , 4 m o l
Áp dụng định luật bảo toàn nguyên tố đối với oxi suy ra:
n O 2 k k = 2. n C O 2 + n H 2 O 2 = 0 , 75 m o l ⇒ n N 2 k k = 0 , 75.4 = 3 m o l .
→ n N ( h c h c ) = 2. ( 69 , 44 22 , 4 − 3 ) = 0 , 2 m o l ⇒ n C : n H : n N = 0 , 4 : 1 , 4 : 0 , 2 = 2 : 7 : 1
Căn cứ vào các phương án ta thấy công thức của X là C 2 H 5 N H 2 .
Đáp án cần chọn là: A

Đáp án : C
nCO2 = 0,4 mol ; nH2O = 0,7 mol , nN2 = 3,1 mol
Bảo toàn O : 2nO2 = 2nCO2 + nH2O => nO2 = 0,75 mol
=> nN2(kk) = 4nO2 = 3 mol => nN2 (sp) = 0,1 mol
=> nC : nH : nN = 0,4 : 1,4 : 0,2 = 2 : 7 : 1
=> C2H7N => 2 đồng phân C2H5NH2 ; CH3NHCH3
=> mX = mC + mH + mN = 9g

Chọn đáp án B.
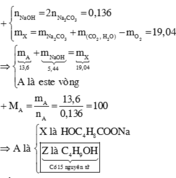
Đốt muối cần số mol O2 =1,165 - 0,785 = 0,38 mol
· Có

⇒ n O ( muối ) = 2 . 0 , 22 = 0 , 44 mol
→ BTNT n H 2 O = 0 , 44 + 2 . 0 , 38 - 3 . 0 , 11 - 2 . 0 , 31 = 0 , 25 mol
![]()
→ BTNT O n CO 2 trong ancol = 0 , 22 + 2 . 0 , 785 - 0 , 71 2 = 0 , 54 mol
![]()
=12.(0,11+0,31+0,54) + 1.(2.0,25+2.0,71-0,22) +16.0,44 =20,26 gam

Chọn đáp án B.
Đốt muối cần số mol O2 = 0,38 mol
· Có n N a O H = 2 n N a 2 C O 3 = 2 . 11 , 66 106 = 0 , 22 m o l
⇒ n O m u ô í = 2 . 0 , 22 = 0 , 44 m o l
→ B T N T N n H 2 O = 0 , 25 m o l
· n O a n c o l = n N a O H = 0 , 22 m o l
→ B T N T O n C O 2
= 0 , 22 + 2 . 0 , 785 - 0 , 71 2 = 0 , 54 m o l
→ B T K L m E = m C + m H + m O = 20,26 g
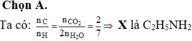

Ta có: \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{12,6}{18}=0,7\left(mol\right)\Rightarrow n_H=0,7.2=1,4\left(mol\right)\)
\(n_{N_2}=\dfrac{69,44}{22,4}=3,1\left(mol\right)\)
BTNT O, có: \(2n_{O_2}=2n_{CO_2}+n_{H_2O}\Rightarrow n_{O_2}=0,75\left(mol\right)\)
\(\Rightarrow n_{N_2\left(trongkk\right)}=\dfrac{0,75}{20\%}.80\%=3\left(mol\right)\)
⇒ nN2 thu được khi đốt A = 3,1 - 3 = 0,1 (mol) ⇒ nN = 0,1.2 = 0,2 (mol)
Gọi: CTPT của A là CxHyNt
⇒ x:y:t = 0,4:1,4:0,2 = 2:7:1
→ CTPT của A có dạng (C2H7N)n
Mà: MA = 45 (g/mol)
\(\Rightarrow n=\dfrac{45}{12.2+7+14}=1\)
Vậy: A là C2H7N.