Cho một hỗn hợp A gồm khí H2 , O2 , COx . Trong hỗn hợp A khí H2 và O2 chiếm lần lượt là 50% và 25% về thể tích . Mắt khác COx chiếm 55% về khối lượng trong A . Biết rằng các khí đo ở cùng điều kiện nhiệt độ và áp suất . Hãy xác định CTHH của COx và tính tỷ khối của A với khí metan ( CH4)


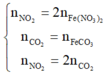

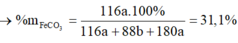
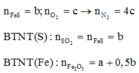
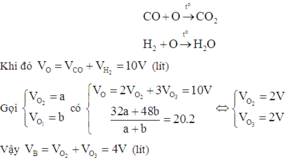

A chứa 50% H2 và 25% O2 và 100 - 50 - 25 = 25% COx
→ Gọi: \(\left\{{}\begin{matrix}n_{H_2}=0,5a\left(mol\right)\\n_{O_2}=0,25a\left(mol\right)\\n_{CO_x}=0,25x\left(mol\right)\end{matrix}\right.\)
Mà: \(\%m_{CO_x}=55\%\) \(\Rightarrow\dfrac{0,25a.\left(12+16x\right)}{0,5a.2+0,25a.32+0,25a\left(12+16x\right)}=0,55\)
\(\Rightarrow\dfrac{0,25.\left(12+16x\right)}{0,5.2+0,25.32+0,25.\left(12+16x\right)}=0,55\)
\(\Rightarrow x=2\)
Vậy: CTHH cần tìm là CO2.
Ta có: \(\overline{M}_A=\dfrac{0,5a.2+0,25a.32+0,25a.44}{0,5a+0,25a+0,25a}=21\left(g/mol\right)\)
\(\Rightarrow d_{A/CH_4}=\dfrac{21}{12+4.1}=1,3125\)