Đốt cháy hoàn toàn chất hữu cơ A có tỉ lệ khối lượng mC : mO = 3 : 2, thu được khí CO2 và hơi nước theo tỉ lệ thể tích CO2 : H2O = 4 : 3 ở cùng nhiệt độ và áp suất. Xác định CTPT của A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{Y\left(29,12g\right)}=n_{CO_2}=\dfrac{14,08}{44}=0,32\left(mol\right)\)
\(\Rightarrow M_Y=\dfrac{29,12}{0,32}=91\left(g/mol\right)\)
Gọi CTPT của Y là CxHyOzNt.
\(\Rightarrow x:y:z:t=\dfrac{14,4}{12}:\dfrac{3,6}{1}:\dfrac{12,8}{18}:\dfrac{5,6}{14}=1,2:3,6:0,8:0,4=3:9:2:1\)
\(\Rightarrow\) CTĐGN của Y là (C3H9O2N)n (n nguyên dương)
\(\Rightarrow n=\dfrac{91}{12.3+9+16.2+14}=1\left(tm\right)\)
Vậy: CTPT của Y là C3H9O2N.

1. 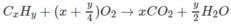
Theo đầu bài ta có: 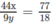
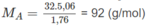
Tức là 12x + y = 92,0 ⇒ x = 7 ; y = 8
Công thức phân tử chất A là C 7 H 8 .
2. Công thức cấu tạo
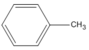 (metylbenzen (toluen))
(metylbenzen (toluen))

Ta có: \(n_{O_2}=\dfrac{2,856}{22,4}=0,1275\left(mol\right)\)
\(\dfrac{V_{CO_2}}{V_{H_2O}}=\dfrac{4}{3}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{4}{3}\)
Gọi: nCO2 = 4x (mol) ⇒ nH2O = 3x (mol)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O
⇒ 2,82 + 0,1275.32 = 4x.44 + 3x.18
⇒ x = 0,03
⇒ nCO2 = 0,03.4 = 0,12 (mol) = nC
nH2O = 0,03.3 = 0,09 (mol) ⇒ nH = 0,09.2 = 0,18 (mol)
Ta có: mC + mH = 0,12.12 + 0,18.1 = 1,62 (g) < 2,82 (g)
→ A chứa C, H và O.
⇒ mO = 2,82 - 1,62 = 1,2 (g) \(\Rightarrow n_O=\dfrac{1,2}{16}=0,075\left(mol\right)\)
Gọi CTPT của A là CxHyOz
⇒ x:y:z = 0,12:0,18:0,075 = 8:12:5
→ CTPT của A có dạng là (C8H12O5)n (n nguyên dương)
Mà: \(M_A< 29.7=203\left(g/mol\right)\)
\(\Rightarrow\left(12.8+12.1+16.5\right)n< 203\)
⇒ n < 1,08 ⇒ n = 1
Vậy: CTPT của A là C8H12O5.

Thông thường khi đề bài cho số mol O2 cần để đốt cháy thì chắc chắn ta sẽ phải sử dụng hoặc định luật bảo khối lượng, hoặc bảo toàn nguyên tố Oxi.
Quay trở lại bài toán này, ta thấy đề cho cần dùng 1,904 lít O2, không cho khối lượng CO2 và H2O mà chỉ cho tỉ lệ thể tích (tỉ lệ số mol), do đó nhận ra được nếu ta sử dụng phương pháp bảo toàn khối lượng ta sẽ tính được số mol CO2 và số mol H2O, từ đó tính được số mol O trong A. Tiếp theo đó ta sẽ xác định công thức đơn giản nhất để tìm ra công thức phân tử.
Có: n O 2 = 1 , 904 22 , 4 = 0 , 085 ( m o l ) ⇒ m O 2 = 0 , 085 . 32 = 2 , 72 ( g a m )
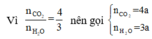
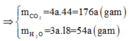
Sơ đồ phản ứng: A + O2 ⇒ CO2 + H2O
Áp dụng định luật bảo toàn khối lượng ta có: m A + m O 2 = m C O 2 + m H 2 O
Hay 1,88 + 2,72 = 176a + 54a ⟺ a = 0,02
⇒ 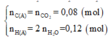
![]()
![]()
Vì C : H : O = nC : nH : nO =0,08 : 0,12 : 0,05 = 8 : 12 : 5
Nên công thức đơn giản nhất của A là C8H12O5.
Khi đó công thức phân tử của A có dạng (C8H12O5)n
Mà MA < 7Mkhôngkhí nên 188n < 7.29 ⇒ n < 1,08 ⇒ n = l
Do đó công thức phân tử của A là C8H12O5.
Đáp án A.

Ta có \(n_{CO_2}=\dfrac{8,8}{44}=0,2(mol);n_{H_2O}=\dfrac{3,6}{18}=0,2(mol)\)
Bảo toàn C và H: \(n_{C}=0,2(mol);n_{H}=0,4(mol)\)
\(\Rightarrow m_A=m_C+m_H=0,2.12+0,4.1=2,8<6\)
Do đó A chứa O
\(\Rightarrow m_O=6-2,8=3,2(g)\\ \Rightarrow n_O=\dfrac{3,2}{16}=0,2(mol)\)
Đặt \(CTHH_A:C_xH_yO_z\)
\(\Rightarrow x:y:z=0,2:0,4:0,2=1:2:1\\ \Rightarrow CTPT_A:CH_2O\)

a, Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng là tỉ lệ về số mol.
Cho: nCO2 = 2 (mol), nH2O = 3 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 3 - 2 = 1 (mol)
Gọi CTPT cần tìm là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=2\)
Vậy: RH là C2H6.
b, Ở cùng điều kiện nhiệt độ, áp suất, tỉ lệ thể tích cũng là tỉ lệ số mol.
Cho nCO2 = 3 (mol), nH2O = 4 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 4 - 3 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=3\)
Vậy: CTPT cần tìm là C3H8.
c, Ta có: \(\dfrac{m_{CO_2}}{n_{H_2O}}=\dfrac{11}{9}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1}{2}\)
Cho nCO2 = 1 (mol), nH2O = 2 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 2 - 1 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=1\)
Vậy: CTPT cần tìm là CH4.
d, Ta có: \(\dfrac{m_{CO_2}}{n_{H_2O}}=\dfrac{44}{27}\Rightarrow\dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{2}{3}\)
Cho nCO2 = 2 (mol), nH2O = 3 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 3 - 2 = 1 (mol)
Gọi CTPT của RH là CnH2n+2.
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=2\)
Vậy: RH là C2H6.
e, Ta có: \(\dfrac{V_{H_2O}}{V_{CO_2}}=1,2\Rightarrow\dfrac{n_{H_2O}}{n_{CO_2}}=1,2=\dfrac{6}{5}\)
Cho nCO2 = 5 (mol), nH2O = 6 (mol)
→ nH2O > nCO2 ⇒ RH là ankan, nRH = 6 - 5 = 1 (mol)
Gọi CTPT của RH là CnH2n+2
\(\Rightarrow n=\dfrac{n_{CO_2}}{n_{RH}}=5\)
Vậy: CTPT cần tìm là C5H12

1. C 2 H 4 O .
2. Số mol A trong 1,10 g A = số mol O 2 trong 0,40 g O 2
n
O
2

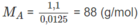
( C 2 H 4 O ) n = 88 ⇒ 44n = 88 ⇒ n = 2
CTPT là C 4 H 8 O 2 .

\(n_{CO_2}=\dfrac{4.4}{44}=0.1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_O=3-0.1\cdot12-0.1\cdot2=1.6\left(g\right)\)
\(n_O=\dfrac{1.6}{16}=0.1\left(mol\right)\)
\(CT:C_xH_yO_z\)
\(x:y:z=0.1:0.2:0.1=1:2:1\)
\(CTnguyên:\left(CH_2O\right)_n\)
\(M_A=\dfrac{3}{\dfrac{1.6}{16}}=30\left(đvc\right)\)
\(\Leftrightarrow30n=30\)
\(\Leftrightarrow n=1\)
\(CTPT:CH_2OhayHCHO\)
Tỉ lệ về thể tích bằng tỉ lệ về số mol
Coi $n_{CO_2} = 4(mol) \Rightarrow n_{H_2O} = 3(mol)$
Bảo toàn nguyên tố C, H :
$n_C = n_{CO_2} = 4(mol) ; n_H = 2n_{H_2O} = 6(mol)$
$m_C = 4.12 = 48(gam)$
$\Rightarrow m_O = 48.\dfrac{2}{3} = 32(gam)$
$\Rightarrow n_O = \dfrac{32}{16} = 2(mol)$
Ta có :
$n_C : n_H : n_O = 4 : 6 : 2 = 2 : 3 : 1$
Vậy CTPT của A là $(C_2H_3O)_n$
Với n = 2 thì tồn tại CTCT : $OH-CH_2-C \equiv C-CH_2-OH$
Vậy CTPT là $C_2H_6O_2$