Phương trình nhiệt hóa học cho biết thông tin gì về phản ứng hóa học.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Phương trình hóa học biểu diễn các phản ứng:
2H2 + O2 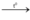 2H2O (pứ hóa hợp + oxi hóa khử)
2H2O (pứ hóa hợp + oxi hóa khử)
4H2 + Fe3O4 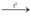 4H2O + 3Fe (pứ thế + oxi hóa khử)
4H2O + 3Fe (pứ thế + oxi hóa khử)
3H2 + Fe2O3 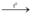 3H2O + 3Fe (pứ thế + oxi hóa khử)
3H2O + 3Fe (pứ thế + oxi hóa khử)
H2 + PbO 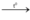 H2O + Pb (pứ thế + oxi hóa khử)
H2O + Pb (pứ thế + oxi hóa khử)
Các phản ứng trên đều là phản ứng oxi – hóa khử vì đều có đồng thời sự khử và sự oxi hóa

\(2H_2+O_2\xrightarrow[]{t^o}2H_2O\\ Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\\ Fe_3O_4+4H_2\xrightarrow[]{t^o}3Fe+4H_2O\\ PbO+H_2\xrightarrow[]{t^o}Pb+H_2O\)

2H2 + O2 -to-> H2O (1)
Fe2O3 + H2 -.to-> 2Fe + 3CO2 (2)
Fe3O4 + 4H2-to-> 3Fe +4H2O (3)
PbO + H2 -to-> Pb + H2O (4)
Các phản ứng trên đều là phản ứng oxi hóa khử
Trong đó, H2 là chất khử vì là chất chiếm oxi của chất khác và O2, Fe3O4, Fe2O3, PbO đều là chất oxi hóa vì là chất nhường oxi cho H2 (phản ứng (1) còn được gọi là phản ứng hóa hợp)

a) Phương trình hóa học biểu diễn ngắn gọn phản ứng hóa học, gồm công thức hóa học của chất phản ứng và sản phẩm phản ứng.
b) Sơ đồ của phản ứng khác với phương trình hóa học là chưa có hệ số thích hợp, tức là chưa cân bằng nguyên tử. Tuy nhiên có một số trường hợp thì sơ đồ cũng là phương trình hóa học.
c) Phương trình hóa học cho biết tỉ lệ về số nguyên tử, số phân tử giữa các chất trong phản ứng cũng như từng cặp chất trong phản ứng.

Ta có:
\(Zn^0-2e\rightarrow Zn^{+2}|3\)
\(S^{+6}+6e\rightarrow S^0|1\)
Vậy ta có PTHH:
\(3Zn+4H_2SO_4--->3ZnSO_4+S+4H_2O\)
\(3Zn+4H_2SO_4->3ZnSO_4+S+4H_2O\)
Chất khử: Zn
Chất oxh: H2SO4
| Zn0-2e-->Zn+2 | x3 |
| S+6+6e --> S0 | x1 |

a)
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2$
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
$Fe_2O_3 + 2Al \xrightarrow{t^o} 2Fe + Al_2O_3$
b) Phản ứng oxi hóa - khử
Chất khử : $CO,H_2,Al$
Chấy oxi hóa : $Fe_2O_3$
c)
$n_{CO} = n_{H_2} = 3n_{Fe_2O_3} = 0,45(mol)$
$V_{CO} = V_{H_2} = 0,45.22,4 = 10,08(lít)$
$n_{Al} = 2n_{Fe_2O_3} = 0,3(mol)$
$m_{Al} = 0,3.27 = 8,1(gam)$
d)
Khối lượng sắt thu được ở phản ứng trên đều như nhau
(Do đều sinh ra Fe với tỉ lệ mol $Fe_2O_3$ : $Fe$ là 1 : 2)

a. \(n_{KClO_3}=\dfrac{18.375}{122,5}=0,15\left(mol\right)\)
PTHH : 2KClO3 ----to---> 2KCl + 3O2
0,15 0,225
Phản ứng trên là phản ứng phân hủy . Vì phản ứng phân hủy là một phản ứng hóa học mà trong đó một chất tham gia có thể tạo thành hai hay nhiều chất mới.
b. \(V_{O_2}=0,225.22,4=5,04\left(l\right)\)
c. \(V_{kk}=5,04.5=25,2\left(l\right)\)

a. \(n_{KMnO_4}=\dfrac{118.5}{158}=0,75\left(mol\right)\)
PTHH : 2KMnO4 -----to----> K2MnO4 + MnO2 + O2
0,75 0,375
Phản ứng trên là phản ứng phân hủy . Vì phản ứng phân hủy là một phản ứng hóa học mà trong đó một chất tham gia có thể tạo thành hai hay nhiều chất mới.
b. \(V_{O_2}=0,375.22,4=8,4\left(l\right)\)
c. \(V_{kk}=8,4.5=42\left(l\right)\)
a) 2KMn04 --> K2MnO4 + MnO2 + O2↑
PƯ này thuộc loại PƯ phân hủy
b) Có nKMnO4 = \(\dfrac{118.5}{39+55+16.4}\)=\(\dfrac{3}{4}\)=0,75
=> nO2 = 0,75x \(\dfrac{1}{2}\)=0,375
=> V của O2 là: 0,375 x 22,4=8,4(l)
c) Thể tích của ko khí là: 1/5 x 8,4=1,68(l)

\(n_{KMnO_4}=\dfrac{118,5}{158}=0,75\left(mol\right)\\
pthh:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,75 0,375
=> \(V_{O_2}=0,375.22,4=8,4\left(l\right)\\
V_{kk}=8,4.5=42\left(l\right)\)

- Phương trình nhiệt hóa học cho biết
+ Phản ứng tỏa nhiệt hay thu nhiệt
+ Trạng thái của các chất đầu (cđ) và sản phẩm (sp)