Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Quá trình tạo thành liên kết cộng hóa trị trong phân tử hydrogen:
+ Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử H liên kết với nhau, mỗi nguyên tử góp chung 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử H cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử hydrogen.
- Quá trình tạo thành liên kết cộng hóa trị trong phân tử oxygen:
+ Nguyên tử O có 6 electron lớp ngoài cùng, cần thêm 2 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử O liên kết với nhau, mỗi nguyên tử góp 2 electron để tạo ra hai cặp electron dùng chung.
+ Hạt nhân của hai nguyên tử O cùng hút các cặp electron dùng chung và liên kết với nhau tạo thành phân tử oxygen.

Gọi ct chung: \(H^I_xS^{II}_y\)
Theo qui tắc hóa trị: `I.x = II.y =>`\(\dfrac{x}{y}=\dfrac{II}{I}\)
`-> x=2, y=1`
`-> CTHH: H_2S`
\(K.L.P.T_{H_2S}=1.2+32=34< amu>.\)
\(\%H=\dfrac{1.2.100}{34}\approx5,88\%\)
`%S = 100%-5,88% =94,12%`

Dựa vào hiệu độ âm điện, trong:
* Na2O: liên kết ion.
* MgO: liên kết ion.
* HBr: liên kết công hóa trị phân cực.
* CaBr2: liên kết ion.

Phân tử đơn chất : O
phân tử liên kết ion: O2
phân tử liên kết cộng hóa trị: H2O
như vầy đc chưa

Na --> Na+ + 1e
S + 2e --> S2-
2 ion Na+ và S2- trái dấu nên hút nhau bởi lực hút tĩnh điện
2Na+ + S2- --> Na2S

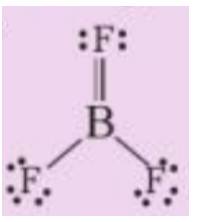
a) Phương trình hóa học: 2B + 3F2 → 2BF3
b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п)
=> Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п

Đáp án C
Các phát biểu đúng là (a); (b)
Phát biểu c sai vì các chất có cùng công thức phân tử nhưng có công thức cấu tạo khác nhau là đồng phân của nhau.
Phát biểu d sai vì phản ứng hữu cơ thường xảy ra chậm và không theo một hướng xác định.
Phát biểu e sai C 9 H 14 Cl 2 có độ bất bão hòa k = 2, không có vòng benzen trong phân tử.
- Xét phân tử H2S được tạo từ 2 phi kim
+ S có 6 electron ở lớp ngoài cùng
+ H có 1 eelctron ở lớp ngoài cùng
=> Nguyên tử H cần thêm 1 electron và S cần thêm 2 electron để đạt cấu hình electron bền vững của khí hiếm
=> Khi 2 nguyên tử H và 1 nguyên tử S liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử S góp ra 2 electron để tạo ra 2 đôi electron dùng chung
- Xét phân tử PH3 được tạo từ 2 phi kim
+ P có 5 electron ở lớp ngoài cùng
+ H có 1 elctron ở lớp ngoài cùng
=> Nguyên tử H cần thêm 1 electron và P cần thêm 3 electron để đạt cấu hình electron bền vững của khí hiếm
=> Khi 3 nguyên tử H và 1 nguyên tử P liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử P góp ra 3 electron để tạo ra 3 đôi electron dùng chung