Quan sát Hình 5.2, hãy cho biết 3 nguyên tố Sc, Ga và Ge nằm ở vị trí nào trong bảng tuần hoàn của Mendeleev (Hình 5.1).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


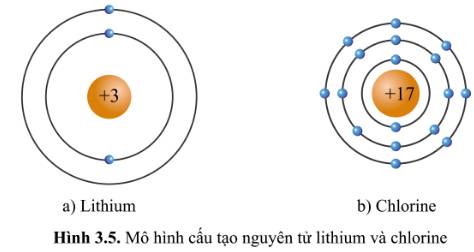
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA

- Vị trí kim loại: nằm ở phía bên trái và góc dưới bên phải của bảng tuần hoàn
- Vị trí phi kim: nằm ở phía trên, bên phải của bảng tuần hoàn
- Vị trí khí hiếm: tất cả các nguyên tố nằm trong nhóm VIIIA

- Nguyên tố carbon:
+ Có số hiệu nguyên tử: 6
+ Nằm ở chu kì 2 => Có 2 lớp electron
- Nguyên tố nhôm:
+ Có số hiệu nguyên tử: 13
+ Nằm ở chu kì 3 => Có 3 lớp electron

- Nguyên tố X nằm ở chu kì 2, nhóm VA => Hàng số 2, cột VA
=> Nguyên tố phosphorus
+ Tên nguyên tố: Phosphorus
+ Kí hiệu hóa học: P
+ Khối lượng nguyên tử: 31
+ Ví trí ô của nguyên tố trong bảng tuần hoàn = số hiệu nguyên tử = 15
+ Ô nguyên tố có màu hồng => Phi kim

- Cấu hình electron của Na (Z = 11): 1s22s22p63s1
- Trong bảng tuần hoàn, Na nằm ở ô số 11, chu kì 3, nhóm IA.
⟹ Ta thấy:
+ Số hiệu nguyên tử = số thứ tự ô = 11
+ Số lớp electron = số thứ tự chu kì = 3
+ Số electron lớp ngoài cùng = số thứ tự nhóm = 1e

- Nguyên tử N nằm ở ô số 7, nhóm VA => Có 5 electron ở lớp ngoài cùng, cần 3 electron để đạt cấu hình khí hiếm
- Nguyên tử C nằm ở ô số 6, nhóm IVA => Có 4 electron ở lớp ngoài cùng, cần 4 electron để đạt cấu hình khí hiếm
- Nguyên tử O nằm ở ô số 8, nhóm VIA => Có 6 electron ở lớp ngoài cùng, cần 2 electron để đạt cấu hình khí hiếm
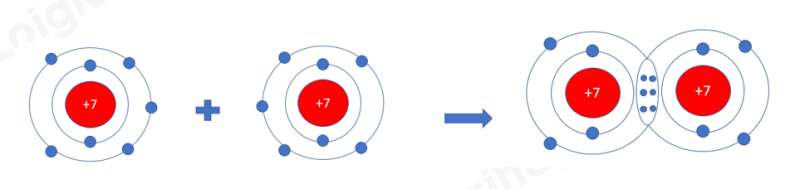
a) Xét phân tử Nitrogen: gồm 2 nguyên tử N
=> Liên kết cộng hóa trị, mỗi N góp 3 electron tạo thành 3 cặp electron dùng chung
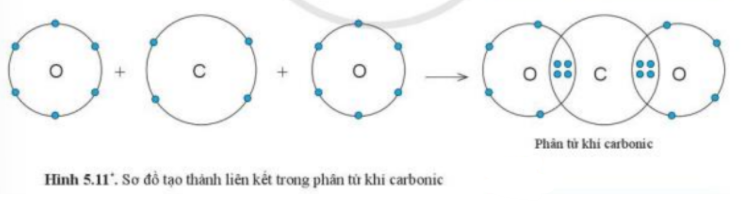
b) Xét phân tử Carbon dioxide: gồm 1 nguyên tử C và 2 nguyên tử O
=> Liên kết cộng hóa trị. Khi C kết hợp với O, nguyên tử C góp 4 electron, mỗi nguyên tử O góp 2 electron
=> Giữa nguyên tử C và nguyên tử O có 2 cặp electron dùng chung

Đáp án A
Vì M – 2e –> M2+ do đó cấu hình electron phải là 1s22s22p63s2 và ở ô số 12 chu kì 3 nhóm IIA

D
Nguyên tử của nguyên tố có:
+ 5 lớp electron → nguyên tố ở chu kỳ 5.
+ 4 electron hóa trị, nguyên tố d → nguyên tố ở nhóm IVB.

\(z=9:1s^22s^22p^5\): chu kì 2, nhóm VIIA
\(z=11:1s^22s^22p^63s^1\): chu kì 3, nhóm IA
\(z=15:1s^22s^22p^63s^23p^3\): chu kì 3, nhóm VA
\(z=21:1s^22s^22p^63s^23p^63d^14s^2\): chu kì 4, nhóm IIIB

Vì theo Hình 5.1, các nguyên tố được sắp xếp theo chiều tăng dần của khối lượng nguyên tử. Mà nguyên tử khối của Sc < Ga < Ge nên
- Sc ở vị trí có nguyên tử khối = 45
- Ga ở vị trí có nguyên tử khối = 68
- Ge ở vị trí có nguyên tử khối = 70