Orbital s có dạng
A. hình tròn
B. hình số tám nổi
C. hình cầu
D. hình bầu dục
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


(a) Sai. Các orbital s đều có dạng hình cầu.
(b) Đúng. Electron thuộc các lớp khác nhau, càng xa hạt nhân thì có năng lượng càng cao.
(c) Sai. Các electron thuộc cùng một lớp có năng lượng gần bằng nhau.
(d) Đúng. Các electron thuộc cùng một lớp có năng lượng gần bằng nhau.

a) Mô hình Rutherford – Bohr còn gọi là mô hình hành tinh nguyên tử vì trong mô hình Rutherford – Bohr electron quay xung quanh hạt nhân theo các quỹ đạo giống như các hành tinh quay xung quanh Mặt Trời.
b) Theo mô hình hiện đại, xác suất tìm thấy electron ở mỗi thùy trong AO p là khoảng 90%.
c)


F2 thu dc:F2:901 quả dỏ,hình tròn:299,hình bầu dục :301 quả vàng ,hình tròn : 103 quả vang,hình bầu dục~9:3:3:1
=> tuân theo quy luật phân li đọc lập Menden
vì cho lai đỏ,tròn x vàng,bầu dục thu dc F1 toàn đỏ,tròn
=> tính trạng đỏ THT so với tính trạng vàng
=> tính trạng tròn THT so với tính trạng bầu dục
Quy ước gen: A quả đỏ a quả vàng
B quả tròn b quả bầu dục
vì cho lai đỏ,tròn x vàng,bầu dục
=> F1 dị hợp; kiểu gen: AaBb
=> P thuần chủng ; kiểu gen: AABB x aabb
P(t/c) AABB( đỏ,tròn) x aabb( vàng,bầu dục)
gp AB ab
F1: AaBb(100% đỏ,tròn)
F1xF1 AaBb( đỏ,tròn) x AaBb(đỏ,tròn)
GF1 AB,Ab,aB,ab AB,Ab,aB,ab
F2:
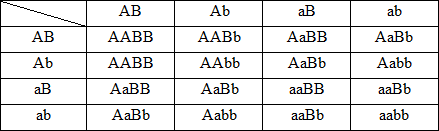
kiểu gen:9A_B_:3A_bb:3aaB_:1aabb
kiểu hình:9 đỏ,tròn:3 đỏ,bầu dục:3 vàng,tròn:1 vàng,bầu dục
C