Câu 7. Cho 6.5g kim loại kẽm phản ứng với 7,3 gam axit clohidric HCl thu được 13,6 gam muối kẽmClorua (ZnC | ) và a gam khí Hidro H) a) Dấu hiệu nào cho thấy có phản ứng hóa học xảy ra? b) Viết sơ đồ phản ứng của phản ứng hóa học trên. c) Viết công thức khối lượng của phản ứng hóa học trên d tính a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Có khí thoát ra
Fe + 2HCl --> FeCl2 + H2
b)
Theo ĐLBTKL: mFe + mHCl = mFeCl2 + mH2
=> mHCl = 25,4 + 0,4 - 11,2 = 14,6(g)

a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)

\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,1 0,1 0,05
b) Lập tỉ số so sánh : \(\dfrac{0,1}{1}>\dfrac{0,1}{2}\)
⇒ Zn dư , HCl phản ứng hết
⇒ Tính toán dựa vào số mol của HCl
\(n_{ZnCl2}=\dfrac{0,1.1}{2}=0,05\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,05.136=6,8\left(g\right)\)
Chúc bạn học tốt

\(a,ĐLBTKL.có.trong.sgk.rồi.tự.học\)
\(b,PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ Áp.dụng.ĐLBTKL,ta.có:\\ m_{Zn}+m_{HCl}=m_{ZnCl_2}+m_{H_2}\\ m_{H_2}=m_{Zn}+m_{HCl}-m_{ZnCl_2}=6,5+7,3-13,6=0,2\left(g\right)\\ n_{H_2}=\dfrac{m}{M}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=n.22,4=0,1.22,4=2,24\left(l\right)\)

a) Lập công thức hóa học của muối kẽm clorua: Z n C l 2
b) Khối lượng muối Z n C l 2 = 6,5 + 7,3 – 0,2 = 13,6 (gam)
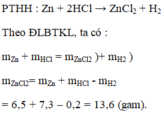
a) Dấu hiệu : Xuất hiện khí không màu không màui
b) $Zn + 2HCl \to ZnCl_2 + H_2$
c) $m_{Zn} + m_{HCl} = m_{ZnCl_2} + m_{H_2}$
$\Rightarrow a = 6,5 + 7,3 - 13,6 = 0,2(gam)$