cho 8,3 g fe và al tác dụng với 500ml dung dịch hcl (d=1,25g/ml) thu được 5,6 lít khí đktc và dung dịch A
a. tính thành phần % khối lượng mỗi kim loại trong hỗn hợp ban đầu
b. tính khối lượng mỗi muối thu được
c. tính khối lượng dung dịch hcl phản ứng
d. tính nồng độ % dung dịch A



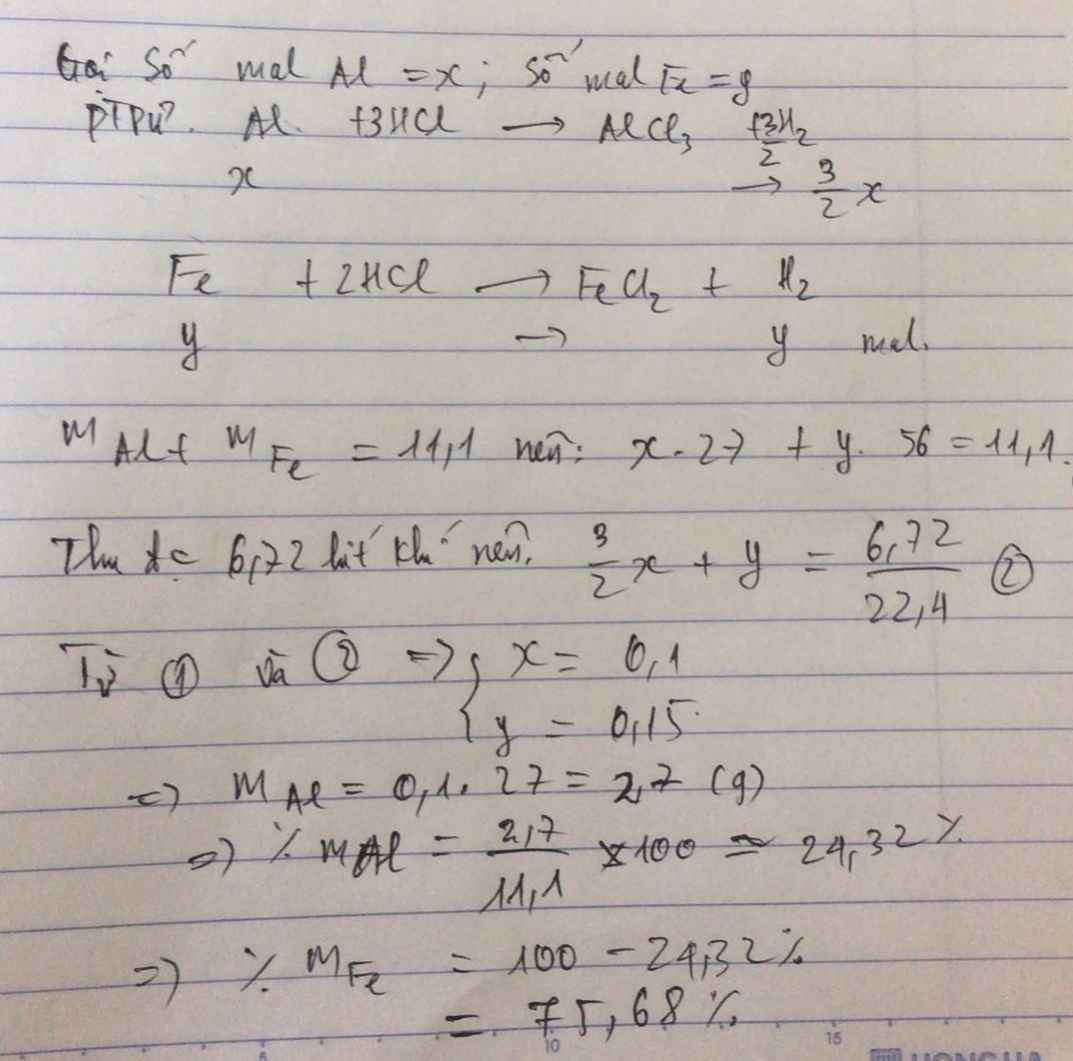
\(Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\)
(mol) x..........2x..........x...........x
\(2Al+6HCl\xrightarrow[]{}2AlCl_3+3H_2\)
(mol) y...........3y............y............1,5y
a) Gọi x, y là số mol Fe, Al
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Ta có hpt: \(\left\{{}\begin{matrix}56x+27y=8,3\\x+1,5y=0,25\end{matrix}\right.\)
⇒ \(\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
\(\%^m_{Fe}=\dfrac{0,1.56}{8,3}.100=67,47\%\)
\(\%^m_{Al}=100-67,47=32,53\%\)
b) \(m_{FeCl_2}=0,1.127=12,7\left(g\right)\)
\(m_{AlCl_3}=0,1.133,5=13,35\left(g\right)\)
c) \(m_{ddHCl}=500.1,25=625\left(g\right)\)
d) Theo BTKL: \(m_{hh}+m_{ddHCl}=m_{ddA}+m_{H_2}\)
⇒ \(m_{ddA}=8,3+625-0,25.2=632,8\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{12,7}{632,8}.100=2\%\)
\(C\%_{AlCl_3}=\dfrac{13,35}{632,8}.100=2,1\%\)