Tính thể tích dung dịch A chứa NaOH 1M; KOH 0,5M cần dùng để trung hòa hết 100 ml dung dịch X gồm H2SO4 0,5M; HNO3 0,1M. Tính khối lượng muối thu được sau phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn đáp án B
n H C l =1 V A ; n H N O 3 = 1 V A ; n H 2 S O 4 =1 V A → n H + =4 V A
n K O H = 1 V A ; n N a O H = 2 V B → n O H - = 3 V B
Để thu được dung dịch có pH= 7 thì n H + = n O H -
→ 4 V A = 3 V B → V A : V B = 3 : 4

\(a.n_{Na_2O}=\dfrac{0,62}{62}=0,01\left(mol\right)\\ Na_2O+H_2O\rightarrow2NaOH\\ n_{NaOH}=2n_{Na_2O}=0,02\left(mol\right)\\ C\%_{NaOH}=\dfrac{0,02.40}{0,62+3,38}.100=20\%\\ b.HCl+NaOH\rightarrow NaCl+H_2O\\ n_{HCl}=n_{NaOH}=0,02\left(mol\right)\\ \Rightarrow V_{HCl}=\dfrac{0,01}{1}=0,01\left(l\right)\)

a) \(M_A=15.2=30\left(g/mol\right)\)
=> A là NO
\(n_{Cu}=\dfrac{0,96}{64}=0,015\left(mol\right)\)
nHNO3 = 0,1.1 = 0,1 (mol)
PTHH: 3Cu + 8HNO3 --> 3Cu(NO3)2 + 2NO + 4H2O
_____0,015->0,04---------->0,015-------->0,01
=> VNO = 0,01.22,4 = 0,224(l)
b) A chứa: 0,015 mol Cu(NO3)2 và 0,06 mol HNO3
=> \(\left\{{}\begin{matrix}Cu^{2+}:0,015\\H^+:0,06\end{matrix}\right.\)
H+ + OH- --> H2O
0,06->0,06
Cu2+ + 2OH- --> Cu(OH)2
0,015->0,03
=> \(n_{OH^-}=0,09\left(mol\right)\) => nNaOH = 0,09 (mol) => \(V_{dd}=\dfrac{0,09}{0,5}=0,18\left(l\right)\)

\(a) 2NaOH + H_2SO_4 \to Na_2SO_4 + H_2O\\ n_{NaOH} = 2n_{H_2SO_4} = 0,1.1.2 = 0,2(mol)\\ \Rightarrow V_{dd\ NaOH} = \dfrac{0,2}{1} = 0,2(lít)\\ b) Na_2SO_3 + H_2SO_4 \to Na_2SO_4 + SO_2 + H_2O\\ n_{SO_2} = n_{Na_2SO_3} = \dfrac{12,6}{126} = 0,1(mol)\\ V_{SO_2} = 0,1.22,4 = 2,24(lít)\)

\(a)n_{MnO_2}=\dfrac{69,6}{87}=0,8mol\\ MnO_2+4HCl\xrightarrow[nhẹ]{đun}MnCl_2+Cl_2+H_2O\)
0,8 3,2 0,8 0,8 0,8
\(V_A=V_{Cl_2}=0,8.22,4=17,92l\\ b)Cl_2+2NaOH\rightarrow NaCl+NaClO+H_2O\)
0,8 1,6 0,8 0,8
\(V_{ddNaOH}=\dfrac{1,6}{1}=1,6l\\ C_{M_{NaCl}}=\dfrac{0,8}{1,6}=0,5M\\ C_{M_{NaClO}}=\dfrac{0,8}{1,6}=0,5M\)
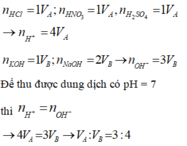
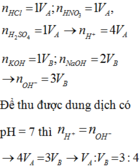
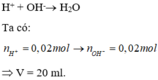

Ta có: \(n_{H_2SO_4}=0,1.0,5=0,05\left(mol\right)\)
\(n_{HNO_3}=0,1.0,1=0,01\left(mol\right)\)
\(\Rightarrow n_{H^+}=0,05.2+0,01=0,11\left(mol\right)\)
Có: \(n_{OH^-}=n_{NaOH}+n_{KOH}=V_{ddA}.1+V_{ddA}.0,5=1,5V_{ddA}\)
PT ion: \(H^++OH^-\rightarrow H_2O\)
\(\Rightarrow1,5V_{ddA}=0,11\) \(\Rightarrow V_{ddA}=\dfrac{11}{150}\left(l\right)\)
Ta có: \(m_m=m_{Na^+}+m_{K^+}+m_{SO_4^{2-}}+m_{NO_3^-}=\dfrac{11}{150}.23+\dfrac{11}{150}.0,5.39+0,05.96+0,01.62\approx8,54\left(g\right)\)