Cho 8,6g h9on hợp Al và Cu tác dụng với dung dịch HCL lấy dư được 6,72 lít khí H2 (đktc). Tính% khối lượng của Al và Cu trong hỗn hợp
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

4 tháng 1 2017
Gọi x, y (mol) lần lượt là số mol Mg, Al trong hỗn hợp.
Phương trình phản ứng:
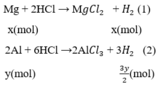
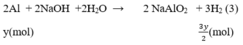
Số mol H2
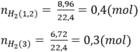
Theo bài ra ta có hệ phương trình:
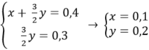
mMg = 24.0,1 = 2,4(g)
mAl = 27.0,2 = 5,4(g)

CX
5 tháng 12 2021
Tham khảo
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
0,2----------------------------------------------0,3
nH2=6,72\22,4=0,3 mol
=>mAl=0,2.27=5,4g

H
20 tháng 10 2021
$2Al + 2H_2O + 2NaOH \to 2NaAlO_2 + 3H_2$
$n_{Al} = \dfrac{2}{3}n_{H_2} = \dfrac{2}{3}. \dfrac{6,72}{22,4} = 0,2(mol)$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Mg + 2HCl \to MgCl_2 + H_2$
$n_{H_2} = \dfrac{3}{2}n_{Al} +n_{Mg}$
$\Rightarrow n_{Mg} = \dfrac{8,96}{22,4} - 0,2.\dfrac{3}{2} = 0,1(mol)$
Suy ra :
$m_{Mg} = 0,1.24 = 2,4(gam) ; m_{Al} = 0,2.27 = 5,4(gam)$
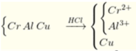
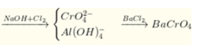
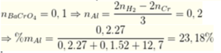
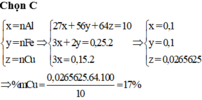
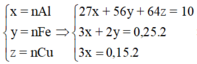
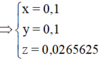
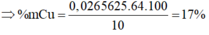
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,6 0,2 0,3
Cu không td với HCl.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
\(\Rightarrow\%_{m_{Al}}=\dfrac{5,4.100}{8,6}=62,79\%\)
\(\Rightarrow\%_{m_{Cu}}=100\%-62,79\%=37,21\%\)