Tổng số hạt trong nguyên tử bằng 40 mà số hạt mang điện nhiều hơn số hạt không mang điện là 10. Tính số hạt proton, neutron, electron.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 1:
\(Z^+=26^+\Rightarrow P=E=Z=26\\ 2P-N=22\Rightarrow N=2P-22=2.26-22=30\)
\(Bài.2:\\ N=35,7\%.28=10\\ \Rightarrow E=P=\dfrac{28-10}{2}=9\)

Số hạt mang điện tích ( p và e ).
( 34 + 10 ) : 2 = 22 ( hạt ).
Mà p = e
=> p = e = 22 : 2 = 11 ( hạt ).
Số hạt không mang điện tích ( n )
22 - 10 = 12 ( hạt )
Vậy nguyên tử đó có p = 11 ; e = 11 ; n = 12.
Số hạt mang điện tích ( p và e ).
( 34 + 10 ) : 2 = 22 ( hạt ).
Mà p = e
=> p = e = 22 : 2 = 11 ( hạt ).
Số hạt không mang điện tích ( n )
22 - 10 = 12 ( hạt )
Vậy nguyên tử đó có p = 11 ; e = 11 ; n = 12.

Gọi kí hiệu của nguyên tử là X
\(p_X+n_X+e_X=37\)
\(\rightarrow2p_X+n_X=37\) (1)
\(2p_X-n_X=11\)(2)
Cộng 1 vào 2 , ta có :
\(4p_X=48\)
\(p_X=e_X=12\)
\(\rightarrow n_X=13\)
--> Mg ( Magie )

Ta có: P = E (Do nguyên tử trung hòa về điện)
- Trong MX3 có tổng số hạt p, e, n là 196.
⇒ 2PM + NM + 3.2PX + 3NX = 196 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 60.
⇒ 2PM + 3.2PX - NM - 3NX = 60 (2)
- Khối lượng nguyên tử X lớn hơn M là 8.
⇒ PX + NX - PM - NM = 8 (3)
- Tổng số hạt trong X- nhiều hơn trong M3+ là 16.
⇒ 2PX + NX + 1 - (2PM + NM - 3) = 16 (4)
Từ (1), (2), (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}P_M=13=Z_M\\N_M=14\\P_X=17=Z_X\\N_X=18\end{matrix}\right.\)
→ M là Al, X là Cl.
Vậy: CTHH cần tìm là AlCl3.

Ta có: P = E (Do nguyên tử trung hòa về điện)
- Tổng số p, e, e trong A và B là 142.
⇒ 2PA + NA + 2PB + NB = 142 (1)
- Tổng số hạt mang điện nhiều hơn số hạt không mang điện là 42.
⇒ 2PA + 2PB - NA - NB = 42 ⇒ NA + NB = 2PA + 2PB - 42 (2)
Thay (2) vào (1), được 4PA + 4PB = 184 (*)
- Số hạt mang điện của B nhiều hơn của A là 12.
⇒ 2PA - 2PB = 12 (**)
Từ (*) và (**) \(\Rightarrow\left\{{}\begin{matrix}P_A=26=Z_A\\P_B=20=Z_B\end{matrix}\right.\)
Vậy: Số hiệu nguyên tử của A và B lần lượt là 26 và 20.

Ta có: P + N + E = 24
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 24 (1)
- Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 8.
⇒ 2P - N = 8 (2)
Từ (1) và (2) ⇒ P = E = N = 8
Cấu hình e: 1s22s22p4
→ Số e lớp ngoài cùng là 6.
Đáp án: A
Đây là nguyên tử oxygen nên số lớp electron ngoài cùng là 6
Chọn: A

Ta có: P + N + E = 34
Mà: P = E (do nguyên tử trung hòa về điện)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11\\N=12\end{matrix}\right.\)

Gọi số hạt proton = số hạt electron = p
Gọi số hạt notron = n
Ta có :
Tổng số hạt : 2p + n = 40
Hạt mang điện nhiều hơn không mang điện là 12 : 2p - n = 12
Suy ra p = 13 ; n = 14
Vậy có 13 hạt proton, 13 hạt electron và 14 hạt notron
bạn ơi mình chưa hiểu lắm lấy 12 : 2p - n số 12 lấy ở đâu vậy ạ mong bn trả lời

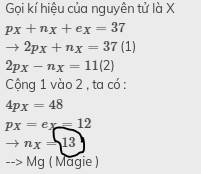
Theo đề: p + e + n = 40
mà p = e => 2p + n = 40 (*)
Mặt khác 2p - n = 10 => \(2p=10+n\), thay vào (*):
\(10+n+n=40\) => n = 15
Thay n = 15 vào (*):
p = e = 12,5 (vô lí) -> đề sai