Cho m (gam) hơi nước qua than nóng đỏ thu được 3,72g hh khí X: H2, CO, CO2. Mặt khác cho 13,44 l hh tác dụng vừa đủ với 40g CuO nung nóng. tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Đặt nCO PT1 = x mol; n C O 2 P T 2 = y mol
C + H2O → t 0 CO + H2
x x mol
C + 2H2O → t 0 CO2 + 2H2
y 2y mol
→nhỗn hợp X = nCO + n C O 2 + n H 2 = 2x+ 3y= 17,92/22,4 = 0,8 mol (*)
CO2+ Ba(OH)2 → BaCO3+ H2O
n C O 2 = n B a C O 3 = 35,46/197 = 0,18 mol
→ y = 0,18 mol
Thay vào (*) ta có x = 0,13 mol
Khí thoát ra là CO (0,13 mol); H2 (x+2y = 0,49 mol)
CO + CuO → t 0 Cu + CO2 (4)
x x
H2 + CuO → t 0 Cu + H2O (5)
(x+2y) (x+2y) mol
Khối lượng chất rắn giảm chính là khối lượng oxi trong oxit tách ra
Theo PT (4,5) ta có: nO (Oxit tách ra) = nCO+ n H 2 = x+x+2y = 0,62 mol
→m = 0,62.16 = 9,92 gam

Đáp án : D
H2(CO) + CuO -> Cu + H2O(CO2)
=> mgiảm = mO pứ = 1,6g => nO pứ = nH2 + nCO = 0,1 mol
C + H2O -> CO + H2
.x -> x -> x
C + 2H2O -> CO2 + 2H2
.y -> y -> 2y
=> 2x + 2y = nCO + nH2 = 0,1 mol => x + y = 0,05 mol
=> m = 0,6g

Ta có mCuO giảm = mO đã bị C lấy đi = 1,6 gam.
⇒ nO bị lấy = 1,6÷16 = 0,1 mol.
Mà ta có: C + 2O → CO2↑.
⇒ nC = 0,1÷2 = 0,05 mol.
⇒ mC = 0,05×12 = 0,6 gam
Đáp án A

Đáp án A
Ta có mCuO giảm = mO đã bị C lấy đi = 1,6 gam.
⇒ nO bị lấy = 1,6÷16 = 0,1 mol.
Mà ta có: C + 2O → CO2↑.
⇒ nC = 0,1÷2 = 0,05 mol.
⇒ mC = 0,05×12 = 0,6 gam

Đáp án B
C + H 2 O → t 0 C O + H 2 ( 1 ) 0 , 042 → 0 , 042 m o l C + 2 H 2 O → t 0 C O 2 + 2 H 2 ( 2 ) 0 , 014 ← ( 0 , 07 - 0 , 042 ) C O 2 + C a ( O H ) 2 → C a C O 3 + H 2 O ( 3 ) C O + C u O → t 0 C u + C O 2 ( 4 ) 0 , 042 ← ( 0 , 112 - 0 , 07 ) H 2 + C u O → t 0 C u + H 2 O ( 5 ) 0 , 07 0 , 07 ← 0 , 07
Ta có: nCuO= 0,112 mol; n H 2 O = 0,07 mol
Tính toán theo phương trình ta có: 0,042 mol CO; 0,014 mol CO2; 0,07 mol H2
% V C O 2 = % n C O 2 = n C O 2 n X . 100 % = 0 , 014 0 , 014 + 0 , 042 + 0 , 07 . 100 % = 11 , 11 %

Đáp án C
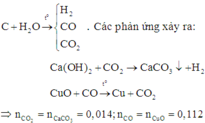
Áp dụng định luật bảo toàn nguyên tố cho nguyên tố C, ta có: n C = n C O + n C O 2 = 0 , 126
Áp dụng định luật bảo toàn mol electron, ta có: 2 n C O + 4 n C O 2 = 2 n H 2 O ⇒ n H 2 O = n C O + 2 n C O 2 = 0 , 14
Vậy tỉ lệ % theo thể tích của CO2 trong A là:
% V C O 2 = 0 , 014 0 , 014 + 0 , 112 + 0 , 14 . 100 % = 5 , 26 %

Giải:
\(H2O+C\rightarrow CO+H2\)
x x x
\(2H2O+C\rightarrow CO2+2H2\)
2y y 2y
Theo phương trình và theo giả thiết ta có: \(2x+3y=0,7\left(1\right)CO+CuO\rightarrow CO2+Cu\)
\(H2+CuO\rightarrow H2O+Cu\)
Áp dụng bảo toàn electron ta có: \(2nCO+2nH2=2nCu=3nNO\rightarrow nCO+nH2=0,6mol\rightarrow\\ 2x+2y=0,6\left(2\right)\)
Từ các phương trình (1), (2) ta có: \(x=\frac{0,2}{y}=0,1\)
Vậy \(\%CO=28,57\%\)
C + H2O →CO + H2
a a a
C + 2H2O →CO2 + 2H2
b b 2b
CO + CuO→ Cu +CO2 a a
H2 + CuO→ Cu +H2O
a +2b a+2b
CuO + H2SO4→CuSO4 + H2O
Cu + H2SO4→CuSO4 + SO2 + H2O
0,6 0,6
n SO2 = 0,6 mol, nX = 0,7
2a + 3b = 0,7
2a + 2b = 0,6
Giải hệ: a= 0,2 mol và b= 0,1 mol
%VCO= 28,57


Gọi $n_{H_2} = a(mol) ; n_{CO} = b(mol) ; n_{CO_2} = c(mol)$
$\Rightarrow 2a + 28b + 44c = 3,72(1)$
Mặt khác :
$n_{hh} = \dfrac{13,44}{22,4} = 0,6(mol)$
$H_2 + CuO \xrightarrow{t^o} Cu + H_2O$
$CO + CuO \xrightarrow{t^o} Cu + CO_2$
$n_{CuO} = n_{H_2} + n_{CO}$
Ta có : $\dfrac{a + b + c}{a + b} = \dfrac{0,6}{0,5}$
$\Rightarrow -0,1a -0,1b + 0,5c = 0(2)$
$C + H_2O \xrightarrow{t^o} CO + H_2$
$C + 2H_2O \xrightarrow{t^o} CO_2 + 2H_2$
Theo PTHH : $n_{H_2} = n_{CO} + 2n_{CO_2}$
$\Rightarrow a = b + 2c(3)$
Từ (1)(2)(3) suy ra : a = 0,14 ; b = 0,06 ; c = 0,04
$n_{H_2O} = n_{H_2} = 0,14(mol)$
$m = 0,14.18 = 2,52(gam)$
\(n_X=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Đặt \(\left\{{}\begin{matrix}n_{H_2}=x\\m_{CO}=y\\n_{CO_2}=z\end{matrix}\right.\) ( mol )
\(\Rightarrow n_X=x+y+z=0,6\left(mol\right)\left(1\right)\)
\(C+H_2O\rightarrow\left(t^o\right)CO+H_2\)
\(C+2H_2O\rightarrow\left(t^o\right)CO_2+2H_2\)
\(Cu+\left\{{}\begin{matrix}CO\\H_2\end{matrix}\right.\rightarrow\left(t^o\right)CuO+\left\{{}\begin{matrix}CO_2\\H_2\end{matrix}\right.\)
\(n_{CuO}=x+y=\dfrac{40}{80}=0,5\left(mol\right)\left(2\right)\)
\(n_{H_2}=n_{CO}+2n_{CO_2}\)
\(\Rightarrow x=y+2z\left(3\right)\)
\(\left(1\right);\left(2\right);\left(3\right)\rightarrow\left\{{}\begin{matrix}x=0,35\\y=0,15\\z=0,1\end{matrix}\right.\)
\(m_X=m_{H_2}+m_{CO}+m_{CO_2}\)
\(=0,35.2+0,15.28+0,1.44=9,3\left(g\right)\)
Bảo toàn H: \(n_{H_2O}=n_{H_2}=0,35\left(mol\right)\) \(\Rightarrow m_{H_2O}=0,35.18=6,3\left(g\right)\)
Ta có: 9,3 gam X `->` 6,3 gam H2O
3,72 gam X `->` 2,52 gam H2O
`=>` \(m=2,52\left(g\right)\)