Nung 15,2 gamhỗnhợp FeO và Fe2O3 trong một bình kín cóchứa 11,2 lít khí CO (đktc). Sau phảnứng hoàn toàn thu được 18 gam hỗnhợp khí.Biếtrằng X bịkhử hoàntoàn thành Fe.a. Xác định thành phần các chất tronghỗnhợp khí.b. Tính khốilượngsắt thuđược và khốilượng 2 oxit banđầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(Đặt:n_{FeO}=a\left(mol\right),,n_{Fe_2O_3}=b\left(mol\right)\)
\(m_X=72a+160b=30.4\left(g\right)\left(1\right)\)
\(FeO+CÒ\underrightarrow{t^0}Fe+CO_2\)
\(Fe_2O_3+3CO\underrightarrow{t^0}2Fe+3CO_2\)
\(X:COdư,CO_2\)
\(m_X=m_{CO\left(dư\right)}+m_{CO_2}=\left(1-a-3b\right)\cdot28+\left(a+3b\right)\cdot44=36\left(g\right)\)
\(\Leftrightarrow16a+48b=8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.1\)
\(m_{Fe}=\left(0.2+0.1\cdot2\right)\cdot56=22.4\left(mol\right)\)
\(m_{FeO}=0.2\cdot72=14.4\left(g\right)\)
\(m_{Fe_2O_3}=0.1\cdot160=16\left(g\right)\)

Đáp án A
Quy hỗn hợp X chứa hai chất: FeO xmol và Fe2O3 y mol
Cho X+ khí CO→Chất rắn Y + khí Z chứa CO, CO2
CO2+ Ca(OH)2 → CaCO3+ H2O
Có: nCO2= nCaCO3= 0,04 mol
Cho Y + H2SO4 đặc nóng dư thu được nSO2=0,045 mol
- Quá trình cho e:
FeO → Fe3++ 1e
x x mol
C+2 → C+4+ 2e
0,04 0,08 mol
- Quá trình nhận electron:
S+6+ 2e → SO2
0,09← 0,045 mol
Theo định luật bảo toàn electron:
ne cho= ne nhận → x+0,08 = 0,09→ x= 0,01mol
Muối thu được sau phản ứng là Fe2(SO4)3
→ nFe2(SO4)3= 18/400= 0,045 mol
Bảo toàn nguyên tố Fe ta có:
x+ 2y= 0,045.2→ y= 0,04 mol
→ m= mFeO + mFe2O3=72x + 160y= 72.0,01+ 160.0,04= 7,12 gam

Đáp án B
Sau khi hỗn hợp X bị CO lấy
đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron:
3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3:
200a = 18 (2)
+ Giải hệ (1) và (2) ta có:
a = b = 0,09 mol
⇒ mY = 0,09(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi
= 6,48 + 0,04×16 = 7,12 gam

Sau khi hỗn hợp X bị CO lấy đi 1 phần oxi ⇒ Chất rắn Y.
+ Đặt nFe/Y = a và nO/Y = b ta có:
PT bảo toàn electron: 3a – 2b = 2nSO2 = 0,09 mol (1)
PT theo muối Fe2(SO4)3: 200a = 18 (2)
+ Giải hệ (1) và (2) ta có: a = b = 0,09 mol
⇒ mY = 0,09×(56+16) = 6,48 gam.
+ Mà nO bị lấy đi bởi CO = nCaCO3 = 0,04 mol
⇒ nX = mY + mO bị lấy đi = 6,48 + 0,04×16 = 7,12 gam
Đáp án B




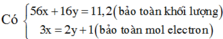
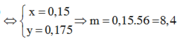
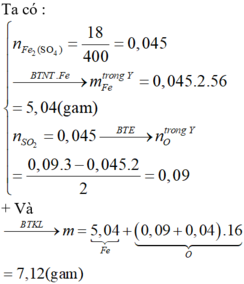
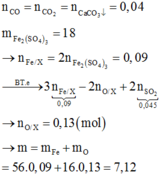
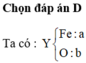
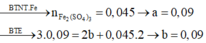

\(Đặt:n_{CO\left(p.ứ\right)}=a\left(mol\right)\left(a>0\right)\\PTHH:FeO+CO\rightarrow \left(t^o\right)Fe+CO_2\\ Fe_2O_3+3CO\rightarrow\left(t^o\right)2Fe+3CO_2\\ hh.khí:CO\left(dư\right),CO_2\\ n_{CO_2}=n_{CO\left(p.ứ\right)}=a\left(mol\right)\\ m_{hh.khí}=18\left(g\right)\\ \Leftrightarrow28.\left(0,5-a\right)+44a=18\\ \Leftrightarrow a=0,25\left(mol\right)\\ \Rightarrow X:\%m_{CO_2}=\dfrac{0,25.44}{18}.100\%\approx61,111\%\\ \Rightarrow\%m_{CO\left(dư\right)}\approx38,889\%\\ b,m_{Fe}=m_{oxit}+m_{CO\left(p.ứ\right)}-m_{CO_2}=15,2+0,25.28-0,25.44=11,2\left(g\right)\\ Đặt:n_{FeO}=t\left(mol\right);n_{Fe_2O_3}=n\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}72t+160n=15,2\\t+3n=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}t=0,1\\n=0,05\end{matrix}\right.\\ \Rightarrow m_{FeO}=72t=7,2\left(g\right);m_{Fe_2O_3}=160n=8\left(g\right)\)