Cho 30,6 gam hỗnhợp X gồm Cu và Fe3O4 tác dụngvới 500 ml dung dịch HNO3 loãng, đun nóng và khuấyđều. Sau khi phảnứngxảy ra hoàn toàn, thuđược 1,68 lit khí NO(sảnphẩmkhử duy nhất,ởđktc), dung dịch Y và còn lại 1,2 gam kim loại.a)Viếtphương trình phảnứngxảy ra.b)Tính nồngđộ mol của axit HNO
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : A
Vì còn dư 0,7g kim loại => đó là Cu => dung dịch muối chỉ có Fe2+ ; Cu2+
Gọi nCu pứ = x ; nFe3O4 = y
Qui hỗn hợp phản ứng về : x mol Cu ; 3y mol Fe ; 4y mol O
Bảo toàn e : 2x + 6y = 3nNO + 8y => 2x – 2y = 0,225
Lại có : mX = 64x + 232y + 0,7 = 30,1
=> x = 0,1875 ; y = 0,075 mol
=> muối khan gồm : 0,1875 mol Cu(NO3)2 ; 0,225 mol Fe(NO3)2
=> mmuối khan = 75,75g

Định hướng tư duy giải
Tư duy đi tắt đòn đầu
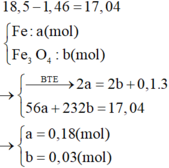
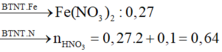
=> [HNO3] = 3,2 (M)

Chọn C.
Ta có: nNO = 0,15 mol.
Gọi a là số mol Cu trong X đã phản ứng; b là số mol Fe3O4 trong X, ta có:
64a + 232b = 61,2 - 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo định luật bảo toàn electron, ta có:
2a + 2.3b - 2.4b = 3.0,15 → a = 0,375; b = 0,15
Muối khan gồm: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
→ mmuối = 188.0,375 + 180.0,45 = 151,5 gam

nNO = 0,15 (mol)
Gọi a là số mol Cu trong X đã phản ứng. Gọi b là số mol Fe3O4 trong X
Ta có: 64a + 232b = 61,2 – 2,4
Các nguyên tố Cu, Fe, O trong hỗn hợp X khi phản ứng với HNO3 chuyển thành muối Cu2+, Fe2+ (vì dư kim loại), H2O do đó theo bảo toàn e: 2a + 2.3b – 2.4b = 3.0,15
Từ đó: a = 0,375; b = 0,15
Muối khan gồm có: Cu(NO3)2 (a = 0,375 mol) và Fe(NO3)2 (3b = 0,45 mol)
mmuối = 188.0,375 + 180.0,45 = 151,5 (gam)
Đáp án B
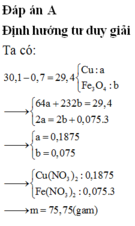

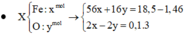
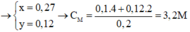

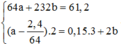
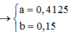
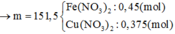
a)
$3Cu + 8HNO_3 \to 3Cu(NO_3)_2 + 2NO + 4H_2O$
$Fe_3O_4 + 10HNO_3 \to 3Fe(NO_3)_3 + NO + 5H_2O$
$2Fe(NO_3)_3 + Cu \to Cu(NO_3)_2 + 2Fe(NO_3)_2$
b) $n_{NO} = \dfrac{1,68}{22,4} = 0,075(mol)$
Gọi $n_{Cu\ pư} = a(mol) ; n_{Fe_3O_4} = b(mol)$
$\Rightarrow 64a + 232b + 1,2 = 30,6(1)$
Bảo toàn electron : $2n_{Cu\ pư} = 2n_{Fe_3O_4} + 3n_{NO}$
$\Rightarrow 2a = 2b + 0,075.3(2)$
Từ (1)(2) suy ra a = 0,1875 ; b = 0,075
$n_{Fe(NO_3)_2} = 3n_{Fe_3O_4} = 0,225(mol)$
$n_{Cu(NO_3)_2} = n_{Cu\ pư} = 0,1875(mol)$
Bảo toàn N : $n_{HNO_3} = 2n_{Fe(NO_3)_2} + 2n_{Cu(NO_3)_2} + n_{NO} = 0,9(mol)$
$C_{M_{HNO_3}} = \dfrac{0,9}{0,5} = 1,8M$
\(a,\) \(3Cu+8HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO+4H_2O\) \(\left(1\right)\)
\(Molx\rightarrow\dfrac{8x}{3}\rightarrow\dfrac{2x}{3}\)
\(3Fe_3O_4+28HNO_3\rightarrow9Fe\left(NO_3\right)_3+NO+14H_2O\) \(\left(2\right)\)
\(Moly\rightarrow\dfrac{28y}{3}\rightarrow3y\rightarrow\dfrac{y}{3}\)
\(2Fe\left(NO_3\right)_3+Cu\rightarrow Cu\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\) \(\left(3\right)\)
Có 1,2 gam kim loại ko tan nên \(Cu\) dư chuyển \(Fe^{3+}\) hết thành \(Fe^{2+}\)
\(b,\) Gọi số mol \(Cu\) phản ứng 1 là x mol, số mol \(Fe_3O_4\) là y mol \(nNO=\dfrac{1,68}{22,4}=0,075mol\)
Theo PT và ĐB ta có
\(\left\{{}\begin{matrix}\dfrac{2x}{3}+\dfrac{y}{3}=0,075\\64\left(x+\dfrac{3y}{2}\right)+232y=30,6-1,2\\\end{matrix}\right.\) ↔ \(\left\{{}\begin{matrix}x=0,075\\y=0,075\end{matrix}\right.\)
Số mol \(HNO_3\) đã dùng là \(\left(\dfrac{8x}{3}+\dfrac{28y}{3}\right)=0,9mol\)
\(\Rightarrow CM\) \(HNO_3=0,9:0,5=1,8M\)
\(#Hoctotnha\)