Tính số phân tử có trong 2,5 mol phân tử nước H2O. Tứ đó, tính số nguyên từ của mỗi nguyên tố có trong lượng chất đó
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) 0,25 mol nguyên tử C có 0,25 × 6,022 × 1023 = 1,5055 × 1023 nguyên tử C.
b) 0,002 mol phân tử I2 có 0,002 × 6,022 × 1023 = 1,2044 × 1021 phân tử I2.
c) 2 mol phân tử H2O có 2 × 6,022 × 1023 = 1,2044 × 1024 phân tử H2O.

Số phân tử nước: 3.6,022.1023= 18,066.1023 (phân tử)
Số nguyên tử H: 2. 18,066.1023= 36,132. 1023 (ng.tử)
Số nguyên tử O = Số phân tử nước: 18,066.1023 (ng.tử)

\(a,\) Số nguyên tử Zn: \(2,5.6.10^{23}=15.10^{23}\)
\(b,\) Số phân tử Na3PO4: \(0,15.6.10^{23}=0,9.10^{23}\)

\(n_{Al_2\left(SO_4\right)_3}=\dfrac{3,42}{342}=0,01\left(mol\right)\\ \Rightarrow n_{Al}=0,01.2=0,02\left(mol\right)\\ n_S=0,01.3=0,03\left(mol\right)\\ n_O=0,01.4.3=0,12\left(mol\right)\)
Số nguyên tử của từng nguyên tố có trong 3,42 gam Al2(SO4)3:
- Số nguyên tử Al: \(0,02.6,02.10^{23}=0,1204.10^{23}\left(nguyên.tử\right)\)
- Số nguyên tử S: \(0,03.6,02.10^{23}=0,1806.10^{23}\left(nguyên.tử\right)\)
- Số nguyên tử O: \(0,12.6,02.10^{23}=0,7224.10^{23}\left(nguyên.tử\right)\)

(a) Phản ứng nổ của TNT: 2C7H5N3O6 → 3N2 + 5H2O + 7CO + 7C
(b) 100 gam thuốc nổ Hexanit có chứa 60 gam TNT và 40 gam HND.
Số mol của từng chất là:
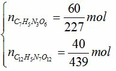
Áp dụng định luật bảo toàn nguyên tố ta có:
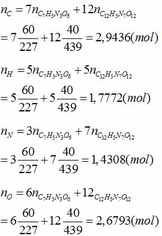
- Phần trăm khối lượng mỗi nguyên tố trong Hexanit:
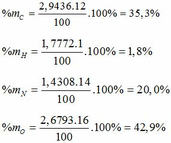
- Sản phẩm nổ của Hexanit là N2, H2O, CO, C
- Áp dụng định luật bảo toàn nguyên tố ta tính được số mol của các chất trong hỗn hợp sau khi nổ:
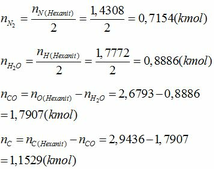
Phần trăm số mol của các chất trong hỗn hợp sau khi nổ:
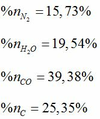

a) 1,5 x 6.1023 = 9.1023 hay 1,5N (nguyên tử Al).
b) 0,5 x 6.1023 = 3.1023 hay 0,5N (phân tử H2).
c) 0,25 x 6.1023 = 1,5.1023 hay 0,25N (phân tử NaCl).
d) 0,05 x 6.1023 = 0,3.1023 hay 0,05N (phân tử H2O).
mAl=nAl.MAl=1,5.27=40,5(g)
mH2=nH2.MH2=0,5.2=1(g)
mNaCl=nNaCl.MNaCl=0,25.(23+35,5)=14,625(g)
mH2O=nH2O.MH2O=0,05.18=0,9

\(n_{SO_3}=\dfrac{2}{80}=0,025\left(mol\right)\\ V_{SO_3}=0,025.22,4=0,56\left(l\right)\\ m_S=0,025.32=0,8\left(g\right)\\ m_O=0,025.48=1,2\left(g\right)\\ 1nguyêntửS,3nguyêntửO\)

`#3107.101107`
a. Sửa đề: Hãy cho biết khối lượng nguyên tử của mỗi nguyên tố có trong phân tử đó.
- Trong phân tử \(\text{SO}_2\) gồm 2 nguyên tử, nguyên tử S và O
`=>` NTK của S là `32` amu, NTK của phân tử O là `16` amu
b.
Khối lượng phân tử của SO2 là:
\(32+16\cdot2=64\left(\text{amu}\right)\)
c.
Số `%` của S có trong SO2 là:
\(\text{%S }=\dfrac{32\cdot100}{64}=50\left(\%\right)\)
Số `%` của O2 có trong SO2 là:
\(\text{%O = 100%}-\text{50% = 50%}\)
Vậy:
a. S: `32` amu, O: `16` amu
b. PTK của SO2 là `64` amu
c. \(\text{%S = 50%; %O = 50%.}\)

Câu 1.
\(M_A=5,31\cdot10^{-23}\cdot6\cdot10^{23}=31,86\approx32\Rightarrow\)A là lưu huỳnh S.
\(n_{H_2O}=\dfrac{0,05}{18}=\dfrac{1}{360}mol\)
Số phân tử H:
\(\dfrac{1}{360}\cdot6\cdot10^{23}=1,67\cdot10^{21}\) nguyên tử

Số phân tử có trong 2,5 mol nước là: \(2,5\cdot6,022\cdot10^{23}=1,5055\cdot10^{24}\) (phân tử)
Số nguyên tử hiđro: \(1,5055\cdot10^{24}\cdot2=3,011\cdot10^{24}\) (nguyên tử)
Số nguyên tử oxi: \(1,5055\cdot10^{24}\) (nguyên tử)