Nguyên tử nguyên tố x có tổng số e trên phân lớp p là 11. Nguyên tử nguyên tố y có số hạt mang điện ít hơn nguyên tử nguyên tố x là 8. a, Viết cấu hình e; sự phân bố e vào các orbital của x và y. b, x và y là kim loại khí hiếm hay phi kim
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Tổng số e trong phân lớp p là 7 => Al
=> tổng số hạt mang điện = 13 + 13 = 26
Trong Y:
Tổng số hạt mang điện = 26 + 8 = 34
=> Z =p = e = 17 => Y là Cl

Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. X có cấu hình 1s22s22p63s23p1 → X là Al (Z= 13)
Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8
→ nguyên tử của nguyên tố Y có số proton hơn số proton trong X là 4
pY=13+4=17 là Cl
Đáp án B.

Đáp án B
Nguyên tử của nguyên tố X có tổng số electron trong các phân lớp p là 7. → X có cấu hình 1s22s22p63s23p1 → X là Al (Z= 13)
Nguyên tử của nguyên tố Y có tổng số hạt mang điện nhiều hơn tổng số hạt mang điện của X là 8
→ nguyên tử của nguyên tố Y có số proton hơn số proton trong X là 4
→ pY = 13 + 4= 17 → Y là Cl
Đáp án B.

Đáp án A
Theo đề bài ta có hệ
2
p
+
n
=
76
2
p
-
n
=
20
→
p
=
4
n
=
28
→ X là Cr (Z= 24). Cấu hình electron của X là [Ar]3d54s1. Đáp án A.

Đáp án A
Theo đề bài ta có hệ 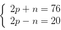 →
→ ![]()
→ X là Cr (Z= 24). Cấu hình electron của X là [Ar]3d54s1. Đáp án A.
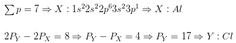
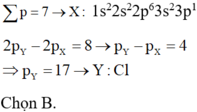
1. Đề chưa chặt chẽ. Đúng ra là ...trên các phân lớp p...
2. Giải: X có cấu hình ...2p6 ...3p5 nên là Clorine có 17p
Y có (17-8)=9p là F cả 2 là phi kim vì có 7 electron ở lớp ngoài cùng. Cấu hình e đầy đủ Cl: 1s22s22p63s23p5 Clo có 3 orbital s chứa 6 e, 6 orbital p chứa 11 e
F: 1s22s22p5 có 2 orbital s chứa 4 e, 3 orbital p chứa 5e