Hoàn thành các phương trình phản ứng sau:
(a) A + B ➝ C + D
(b) C ---a/s,to---> M + N
(c) N + Q ➝ A
Biết A là hợp chất muối của kim loại Q với nguyên tố Clo chiếm 60,683% về khối lượng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) X là Cl2
Z là hợp chất 2 nguyên tố, Z là muối của Kali trong đó chiếm 52,35% về khối lượng => Z là KCl
Y là hợp chất 2 nguyên tố, trong đó có chứa Clo, dd Y làm quỳ tím chuyển sang màu đỏ => Y là axit => Y là HCl
Đất đèn +HCl → F => F là C2H2
Ta có sơ đồ sau:
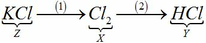

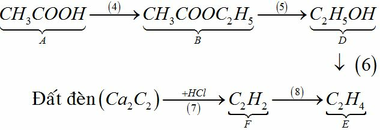
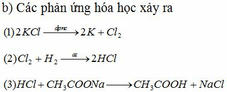
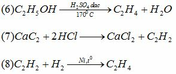
4 C H 3 C O O N a + C 2 H 5 O H ↔ H 2 S O 4 , t ∘ C H 3 C O O C 2 H 5 + H 2 O 5 C H 3 C O O C 2 H 5 + N a O H → C H 3 C O O N a + C 2 H 5 O H

Gọi KL cần tìm là M
\(n_{AgNO_3}=\dfrac{170}{170}=1(mol)\\ MCl_2+2AgNO_3\to M(NO_3)_2+2AgCl\downarrow\\ \Rightarrow n_{MCl_2}=\dfrac{1}{2}n_{AgNO_3}=0,5(mol)\\ \Rightarrow M_{MCl_2}=\dfrac{55,5}{0,5}=111(g/mol)\\ \Rightarrow M_M=111-35,5.2=40(g/mol)(Ca)\\ n_{Ca(NO_3)_2}=0,5(mol);n_{AgCl}=1(mol)\\ \Rightarrow m_{Ca(NO_3)_2}=0,5.164=82(g);m_{AgCl}=1.143,5=143,5(g)\)

Gọi: hóa trị R là n; số mol R phản ứng là x.
2R + nCl2 -> 2RCln (*)
2_____n_____2
x___xn / 2___x (mol)
RCln không phản ứng được với O2.
=> R còn dư.
=> X gồm: RCln và R dư. Gọi số mol R dư là y.
4R + nO2 -> 2R2On (**)
4_____n______2
y___yn / 4____0,5y (mol)
Y là: R2On và RCln.
Theo đề bài, ta có:
>>R(x+y) = 16,2 (m R)
<=> Rx + Ry = 16,2 (1)
>>Ry + RCln.x = 58,8 (m X) (2)
>>R2On.0,5y + RCln.x = 63,6 (m Y) (3)
Lấy (2) trừ (1), được:
RCln.x - Rx = 42,6
Theo phương trình (*), ta thấy:
mCl2 = mRCln - mR
<=> mCl2 = RCln.x - Rx
<=> mCl2 = 42,6
=> n Cl2 = 0,6
=> xn / 2 = 0,6
<=> xn = 1,2 (a)
Lấy (3) trừ (2), được:
R2On.0,5y - Ry = 4,8
Theo phương trình (**), ta thấy:
mO2 = mR2On - mR (dư)
<=> mO2 = R2On.0,5y - Ry
<=> mO2 = 4,8
=> n O2 = 0,15
=> yn / 4 = 0,15
<=> yn = 0,6 (b)
Từ (a) và (b), suy ra:
xn + yn = 1,2 + 0,6 = 1,8
<=> n(x+y) = 1,8
Hóa trị kim loại nhận các giá trị: 1, 2, 3.
Với n = 1 => x+y = 1,8 => R = 16,2 / (x+y) = 16,2 / 1,8 = 9 (Be - loại vì Be hóa trị II).
Với n = 2 => x+y = 0,9 => R = 16,2 / (x+y) = 16,2 / 0,9 = 18 (loại).
Với n = 3 => x+y = 0,6 => R = 16,2 / (x+y) = 16,2 / 0,6 = 27 (Al - nhận vì Al hóa trị III).
Vậy: kim loại R cần tìm là Nhôm (Al).
2Al + 3Cl2 -t*-> 2AlCl3
2_____________2
x_____________x (mol)
4Al + 3O2 -t*-> 2Al2O3
4_____________2
y_____________0,5y (mol)
X gồm: AlCl3 và Al dư.
Y gồm: AlCl3 và Al2O3.
n Al = 16,2 / 27 = 0,6 = x + y.
Ta có hệ phương trình:
x + y = 0,6 (n Al)
133,5x + 27y = 58,8 (m X gồm AlCl3 và Al dư)
Giải hệ, được: x = 0,4; y = 0,2.
=> m AlCl3 = 53,4g
=> m Al dư = 5,4g.
=> % AlCl3 trong X = 90,82%.
=> % Al dư trong X = 9,18%.

%Na = 39,316% => MZ = 58,5
=> Z là NaCl
=> X là H2 và Y là HCl
Pt: Cl2 + H2 → 2HCl
HCl + NaOH → NaCl + H2O
2NaCl + H2SO4đặc → Na2SO4 + 2HCl
4HCl + MnO2 → MnCl2 + Cl2↑ + 2H2O

2. cthc oxit cao nhất của RH3 là R2O5
%R = 100 - 74,07 = 25,93%
\(\dfrac{2M_R}{25,93}=\dfrac{80}{74,07}\)
\(\Rightarrow M_R=14\)
R là Nitơ ( N )
\(Bài1.\)
Gọi hai kim loại đó là A, n là hóa trị trung bình
\(2A+2nHCl\rightarrow2ACl_n+nH_2\)
\(n_{H_2}\left(đkct\right)=0,03\left(mol\right)\)
Theo PTHH: \(n_{HCl}=2n_{H_2}=0,06\left(mol\right)\)
\(\Rightarrow m_{HCl}\left(pứ\right)=0,06.36,5=2,19\left(g\right)\)
Ap dung ĐLBTKL: \(\Rightarrow a=2+2,19-0,03.2=4,13\left(g\right)\)
\(Bài 2.\)
Vì R tạo với Hỉdro hợp chất là RH3
\(\Rightarrow\) R tạo với Oxi hợp chất là \(R_2O_5\)
Theo đề, ta có: \(74,07=\dfrac{16.5.100}{2R+16.5}\)
\(\Rightarrow R< 0\)
Không có kim loại nào thõa đề bài trên
Bạn xem lại đề xem, số liệu ....
\(Bài 3.\)
Gọi R là kim loai có hóa trị I cần tìm:
\(2R+2HCl\rightarrow2RCl+H_2\)
\(n_R=\dfrac{4,6}{R}\left(mol\right)\)
\(n_{H_2}=\dfrac{1,321}{22,4}\left(mol\right)\)
Theo PTHH: \(n_R=2n_{H_2}\)
\(\Leftrightarrow\dfrac{4,6}{R}=\dfrac{2,642}{22,4}\)
\(\Leftrightarrow R=39\left(K\right)\)
Vậy kim loại đó là Kali

a)Gọi A là tên kim loại hóa trị III
2A+3Cl2=>2ACl3
Ta có p.trình:
A/10.8=A+106.5/53.4
<=>53.4A-10.8A=1150.2
<=>42.6A=1150.2;<=>A=27
Vậy A là nhôm
b)MnO2+4HCl=>MnCl2+Cl2+2H20
nAl=10.8/27=0.4mol
=>nCl2=0.4*3/2=0.6mol
=>nCl2(l.thuyết)=0.6*100%/80%=0.75mol
=>mMnO2=0.75*87=65.25(g)
=>mHCl=(0.75*4)*36.5=109.5(g)
=>mddHCl=109.5*100%/37%=295.9(g)
=>VddHCl=255.9/1.19=248.7ml

3. \(n_{Cl_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt: \(M+\dfrac{1}{2}Cl_2\underrightarrow{t^o}MCl\)
M 0,5mol
4,6g 0,1mol
\(\Rightarrow M=23\)
M là Natri ( Na )
\(n_{NaCl}=\dfrac{0,5}{\dfrac{1}{2}}=1\left(mol\right)\)
Pt: \(NaCl+H_2O\rightarrow NaOH+HCl\)
1mol \(\rightarrow1mol\) \(\rightarrow1mol\)
\(C\%_{NaOH}=\dfrac{1.40}{188,3}.100=21,24\%\)
\(C\%_{HCl}=\dfrac{1.36,5}{188,3}.100=19,38\%\)
1.
| Công thức | Gọi tên |
| BaCO3 | Bari cacbonat |
| Na2SO4 | Natri sunfat |
| CuO | Đồng (II) oxit |
| Li2O | Liti oxit |
| H3PO4 | axit photphoric |
| MgSO4 | Magie sunfat |
| FeS | Sắt (II) sunfua |
| Fe(OH)2 | Sắt (II) hidroxit |
| KHS | Kali hidrosunfua |
| Ca(HSO4)2 | Canxi hidro sunfat |
| BaSO4 | Bari sunfat |
K2SiO3 : Kali Silicat
2)Gọi CTTQ hợp chất là:SxOy
x:y=\(\dfrac{24}{32}:\dfrac{36}{16}\)=1:3
=>CTĐG hợp chất là:SO3=>CTN hợp chất là:(SO3)n
Mặt khác:Mh/c=40\(M_{H_2}\)=40.2=80
=>80n=80=>n=1
Vậy CTHH hợp chất là SO3
Gọi CTHH của A là: \(QCl_n\left(n\in N\text{*}\right)\)
\(\rightarrow\dfrac{35,5n}{M_Q+35,5n}.100\%=60,683\%\\ \Leftrightarrow M_Q=23n\left(g/mol\right)\)
Xét n = 1 thoả mãn => MQ = 23 (g/mol)
=> Q là Na
\(\left(a\right)NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\\ \left(b\right)2AgCl\xrightarrow[a/s]{t^o}2Ag+Cl_2\\ \left(c\right)2Na+Cl_2\xrightarrow[]{t^o}2NaCl\)