Lắc kĩ m gam bột Ni (Ni=59) với 150 gam dd gồm AgNO3 8,5% va Cu(NO3)2 14,1%.
a) Tính khối lượng Ni cần dùng để pư vừa hết ion Ag+.
b) Tính khối lượng Ni cần dùng để pư xong, lượng Cu(NO3)2 còn một nửa lượng ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Để tách riêng Ag ra khỏi hỗn hợp Ag, Cu, Ni, Fe mà vẫn giữ nguyên khối lượng của Ag ban đầu thì cần một dung dịch hòa tan được Cu, Ni, Fe mà không hòa tan được Ag, đó chính là dung dịch FeCl3.

Đáp án : C
Dựa vào dãy điện hóa
Đồng thời không là thay đổi khối lượng Ag nên không dùng chất có phản ứng với Ag

Đáp án C
Để tách riêng Ag ra khỏi hỗn hợp Ag, Cu, Ni, Fe mà vẫn giữ nguyên khối lượng của Ag ban đầu thì cần một dung dịch hòa tan được Cu, Ni, Fe mà không hòa tan được Ag, đó chính là dung dịch FeCl3.

Ta có; \(\left\{{}\begin{matrix}n_{Fe}=0,04\left(mol\right)\\n_{AgNO_3}=0,02\left(mol\right)\\n_{Cu\left(NO_3\right)_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(Fe\left(0,01\right)+2AgNO_3\left(0,02\right)\rightarrow Fe\left(NO_3\right)_2\left(0,01\right)+2Ag\left(0,02\right)\)
\(Fe\left(0,03\right)+Cu\left(NO_3\right)_2\left(0,03\right)\rightarrow Fe\left(NO_3\right)_2\left(0,03\right)+Cu\left(0,03\right)\)
Dung dịch B sau phản ứng: \(\left\{{}\begin{matrix}Fe\left(NO_3\right)_2:0,01+0,03=0,04\left(mol\right)\\Cu\left(NO_3\right)_2\left(dư\right)=0,1-0,03=0,07\left(mol\right)\end{matrix}\right.\)
\(V_{ddsau}=200\left(ml\right)=0,2\left(l\right)\)
Suy ra nồng độ mol
Chất rắn A: \(\left\{{}\begin{matrix}Ag:0,02\left(mol\right)\\Cu:0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_A=0,02.108+0,03.64=4,08\left(g\right)\)
Câu này bạn tính hết số mol ra, viết pt, rồi tính theo bài toán dư hết -> đẩy số mol của chất hết sang. Giờ đang bận nên nói gọn vậy nha

Bài 5:
\(\underrightarrow{BT:Fe}n_{Fe}=n_{Fe\left(OH\right)_2}=\dfrac{m}{56}\left(mol\right)\)
\(\rightarrow n_{Fe_2O_3}=\dfrac{m}{112}\left(mol\right)\rightarrow m_{Fe\left(OH\right)_2}=\dfrac{45}{28}m\left(gam\right)\)
mà \(m_{Fe_2O_3}+m_{CuO}=b\rightarrow m_{CuO}=\left(b-\dfrac{10}{7}m\right)gam\)
\(\underrightarrow{BT:Cu}m_{Cu\left(OH\right)_2}=\left(\dfrac{49b-70m}{40}\right)gam\)
Ta có: \(m_{Fe\left(OH\right)_2}+m_{Cu\left(OH\right)_2}=a\rightarrow\dfrac{45m}{28}+\dfrac{49b-70m}{40}\)
\(\rightarrow m=8,575b-7a\)
Vậy chọn đáp án B
Bài 2:
Bảo toàn khối lượng, ta có: \(133,5_{n_{AlCl_3}}+127_{n_{FeCl_2}}=m_{Al}+m_Y-m_{ran}=65,68\left(g\right)\)
Bảo toàn nguyên tố: \(n_{AlCl_3}=n_{Al}=0,32\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{AlCl_3}=0,32\left(mol\right)\\n_{FeCl_2}=0,18\left(mol\right)\end{matrix}\right.\)
Trong Y có: \(\left\{{}\begin{matrix}133,5_{n_{CuCl_2}}=+162,5_{n_{FeCl_3}}=m_Y=74,7\\2n_{CuCl_2}+3n_{FeCl_3}=3n_{AlCl_3}+2n_{FeCl_2}=1,32\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}n_{FeCl_3}=0,36\left(mol\right)\\n_{CuCl_2}=0,12\left(mol\right)\end{matrix}\right.\) Suy ra tỉ lệ là 3:1
Vậy chọn đáp án C
Bài 3:

Bài 4:

Đáp án C
Vì Z chứa 2 muối và T chứa 2 kim loại nên Z chứa Zn(NO3) và Ni(NO3)2, T chứa Ag và Cu.
Do đó cả 4 chất đều phản ứng vừa đủ hết.
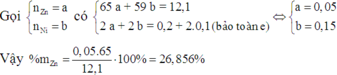

Đáp án D.
![]()
Sau khi pư kết thúc thu đc dd A với màu xanh đã nhạt 1 phần à Fe đã phản ứng hết với AgNO3 và phản ứng với một phần Cu(NO3)2.
Gọi số mol Cu(NO3)2 phản ứng là x mol.
Fe + 2AgNO3 à Fe(NO3)2 + 2Ag
0,06ß 0,12 à 0,12
Fe + Cu(NO3)2 à Fe(NO3)2 + Cu
x ß x à x
Vậy mtăng = 0,12.108 + x.64 – 0,06.56 – x.56 = 10,4 ó x = 0,1 mol
Vậy khối lượng đinh sắt ban đầu là: mFe = 0,1.56 + 0,06.56 = 8,96 gam.
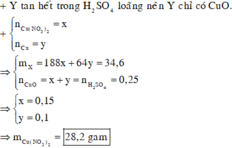

a)
\(n_{AgNO_3}=\dfrac{150.8,5\%}{170}=0,075\left(mol\right)\)
PTHH: Ni + 2AgNO3 --> Ni(NO3)2 + 2Ag
0,0375<-0,075
\(\Rightarrow m_{Ni}=0,0375.59=2,2125\left(g\right)\)
b) \(n_{Cu\left(NO_3\right)_2\left(bđ\right)}=\dfrac{150.14,1\%}{188}=0,1125\left(mol\right)\)
=> \(n_{Cu\left(NO_3\right)_2\left(pư\right)}=0,05625\left(mol\right)\)
PTHH: Ni + 2AgNO3 --> Ni(NO3)2 + 2Ag
0,0375<--0,075
Ni + Cu(NO3)2 --> Ni(NO3)2 + Cu
0,05625<-0,05625
=> mNi = 59(0,0375 + 0,05625) = 5,53125 (g)