Cho 11,7 gam một kim loại X hóa trị II vào 350 ml dung dịch HCl 1M, khi phản ứng kết thúc ta thấy kim loại vẫn còn dư. Mặt khác để hòa tan hoàn toàn lượng kim loại trên phải cần chưa đến 200 ml dung dịch HCl 2M. Tìm X.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
M + H2SO4 → MSO4 + H2 (1)
2KOH + H2SO4 → K2SO4 + 2H2O (2)
![]()
Mà
![]()
![]()
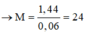
M là Magie

\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15\left(mol\right)\)
\(M+2HCl\rightarrow MCl_2+H_2\)
0,15<-0,3<---0,15<----0,15
a. \(M=\dfrac{8,4}{0,15}=56\left(g/mol\right)\)
Vậy M là kim loại Fe.
b. \(n_{NaOH}=0,5.1=0,5\left(mol\right)\)
\(HCl+NaOH\rightarrow NaCl+H_2O\)
0,2<-----0,2
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2+2NaCl\)
0,15----->0,3
\(m_{dd.HCl}=\dfrac{\left(0,3+0,2\right).36,5.100\%}{10\%}=182,5\left(g\right)\)
\(m_{dd.A}=8,4+182,5-0,15.2=190,6\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{127.0,2.100\%}{190,6}=13,33\%\)
\(C\%_{HCl.dư}=\dfrac{0,3.36,5.100\%}{190,6}=5,75\%\)

- Khi cho 2,4g X vào 200ml ddHCl 0,75M
nHCl = 0,2.0,75 = 0,15 (mol)
....\(X+2HCl\rightarrow XCl_2+H_2\)
0,075.....0,15...............................(mol)
do X còn dư nên \(\dfrac{2,4}{X}>0,075\Leftrightarrow X< 32\) (1)
- Khi cho 2,4g X vào 250ml ddHCl 1M
nHCl = 0,25.1 = 0,25 (mol)
...\(X+2HCl\rightarrow XCl_2+H_2\)
\(\dfrac{2,4}{X}\)......\(\dfrac{4,8}{X}\)..............................(mol)
axit còn dư \(\Rightarrow\dfrac{4,8}{X}< 0,25\Leftrightarrow X>19,2\) (2)
Từ (1) và (2) \(\Rightarrow\) 19,2 < X < 32 mà X là kim loại hóa trị II \(\Rightarrow X=24\)
Vậy kim loại X là Mg

Theo bài ra: nH2 = 1,12/22,4 = 0,05 mol
nHCl < 0,5 x 1 = 0,5 mol
Các phương trình pứ xảy ra:
Fe + 2HCl ===> FeCl2 + H2
N + 2HCl ===> NCl2 + H2 ( đặt công thức chung của hỗn hợp là N)
0,05 0,05 ( giả thiết nhé bạn )
=> MN= 2 / 0,05 = 40 gam
Vì MFe = 56 > 40 => MM < 40 (1)
Mặt khác , ta có: MM > 4,8 / 0,5 = 9,6 (2)
Từ (1), (2), ta có 9,6 < MM < 40 và M hóa trị II
=> M là Magie



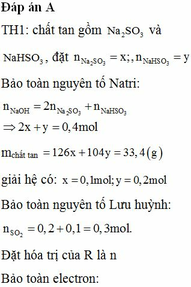

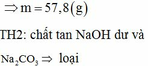
nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s