Bằng kiến thức hóa học, hãy cho biết một chất nào hoặc một cặp chất nào có thể tác dụng với nhau để : a) điều chế hiđro (H²) trong phòng thí nghiệm ? b) tạo thành dung dịch làm quỳ tím hóa đỏ ? c) điều chết khí oxi (O²) trong phòng thí nghiệm? d) chỉ sinh ra oxit ? Viết các phương trình phản ứng hóa học xảy ra và ghi rõ điều kiện ( nếu có ) .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chỉ có HCl tác dụng với MnO2 ở nhiệt độ thường mới điều chế được khí Clo.
Các cặp chất khác đều có nhiệt độ cao.

Câu trả lời đúng là C.
PT: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Từ phản ứng này ⇒ có thể điều chế khí H2
Khí H2 nhẹ hơn không khí nên úp ngược ống nghiệm sẽ thu được khí H2

Đáp án B
- Dung dịch Y làm quì tím hóa xanh
=> trong 4 đáp án thì Na2CO3 thỏa mãn (muối của axit yếu và kiềm mạnh)
- Khi X + Y tạo kết tủa => Chỉ có đáp án B thỏa mãn:
Ba(NO3)2 + Na2CO3 → BaCO3 + 2NaNO3

a) Nước tạo ra dung dịch làm quỳ tím hóa đỏ : SO3
Pt : \(SO_3+H_2O⇌H_2SO_3\)
b) Nước tạo ra dung dịch làm quỳ tím hóa xanh : CaO
Pt : \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
c) Hydro chloric acid HCl tạo khí có mùi hắc : Na2SO3
Pt : \(Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\)
d) Hydro clodric acid HCl tạo ra khí nhẹ nhất và cháy được : Al
Pt : \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
e) Sulfuric acid H2SO4 tạo ra chất kết tủa màu trắng không tan trong axit sinh ra : BaCl2
Pt : \(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
f) Sodium hidroxide NaOH tạo ra chất kết tủa màu nâu đỏ : FeCl3
Pt : \(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
g) Bị nhiệt phân hủy tạo ra chất khí làm đục nước vôi trong : CaCO3
Pt : \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
h) Bị nhiệt phân hủy tạo ra chất rắn màu đen và hơi nước : Cu(OH)2
Pt : \(Cu\left(OH\right)_2\underrightarrow{t^o}CuO+H_2O\)
Chúc bạn học tốt

A là \(P_2O_5\)
\(P_2O_5+3H_2O\to 2H_3PO_4\) làm quỳ hóa đỏ
B là \(Fe\)
\(Fe+2HCl\to FeCl_2+H_2\uparrow\)
D là \(Ba\)
\(Ba+H_2O\to Ba(OH)_2+H_2\uparrow\\ Ba+2HCl\to BaCl_2+H_2\uparrow\)
E là \(BaO\)
\(BaO+H_2O\to Ba(OH)_2\) làm quỳ tím hóa xanh
G là \(Fe_3O_4\text{ hoặc }Fe_2O_3\)
\(Fe_3O_4+4H_2\xrightarrow{t^o}3Fe+4H_2O\\ Fe_2O_3+3H_2\xrightarrow{t^o}2Fe+3H_2O\)

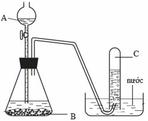
(a) Từ hình ảnh bộ dụng cụ ta thấy đây là bộ dụng cụ để điều chế các khí không tác dụng được với nước, và không tan hoặc rất ít tan trong nước
=> khí C có thể điều chế được là các khí: H2, C2H2, SO2
Cl2 và HCl không điều chế được vì tan trong nước
CO không điều chế được bằng bộ dụng cụ này trong phòng thí nghiệm.
(b)
Điều chế: H2 ; A có thể là HCl hoặc H2SO4 loãng ; B là có thể là kim loại Zn, Fe…
2HCl + Zn → ZnCl2 + H2↑
Điều chế: C2H2; A là H2O ; B là CaC2 rắn
2H2O + CaC2 → Ca(OH)2 + C2H2↑
Điều chế: SO2 ; A là HCl ; B là Na2SO3 rắn
2HCl + Na2SO3 → 2NaCl + SO2↑ + H2O

a. \(2K+2H_2O--->2KOH+H_2\)
b. \(BaO+H_2O--->Ba\left(OH\right)_2\)
\(K_2O+H_2O--->2KOH\)
\(CaO+H_2O--->Ca\left(OH\right)_2\)
\(Li_2O+H_2O--->2LiOH\)
c. \(P_2O_5+3H_2O--->2H_3PO_4\)
\(SO_3+H_2O--->H_2SO_4\)
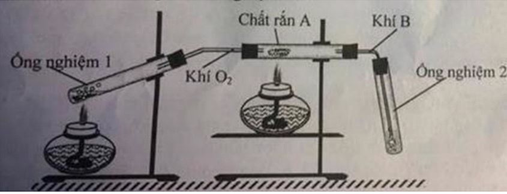
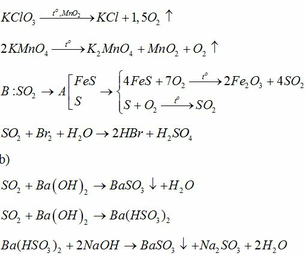
\(a,Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ b,CO_2+H_2O\rightarrow H_2CO_3\\ c,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ C+O_2\underrightarrow{t^o}CO_2\)