Dẫn 1,12 lít hh A(metan và etilen) đo ở đktc qua dd brom thì sau pứ làm mất màu tối đa 40g dd brom 4%.Thành phần % thể tích metan và etilen lần lượt là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Dẫn 2 khí qua dung dịch nước brom chỉ có C 2 H 4 phản ứng
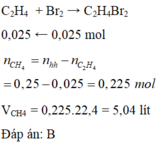

\(n_{hh\left(CH_4,C_2H_4\right)}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{Br_2}=\dfrac{4}{160}=0,025\left(mol\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ n_{C_2H_4}=n_{Br_2}=0,025\left(mol\right)\)
Vì số mol tỉ lệ thuận với thể tích, nên ta có:
\(\%n_{C_2H_4}=\dfrac{0,025}{0,25}.100\%=10\%\\ \Rightarrow\%V_{C_2H_4}=10\%;\%V_{CH_4}=100\%-10\%=90\%\)

\(n_{Br_2}=\dfrac{20}{160}=0,125\left(mol\right)\)
PTHH: C2H4 + Br2 ---> C2H4Br2
0,125 0,125
\(\%V_{C_2H_4}=\dfrac{0,125.22,4}{5,6}=50\%\\ \%V_{CH_4}=100\%-50\%=50\%\)

\(n_{hhkhí\left(C_2H_4,CH_4\right)}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
\(m_{tăng}=m_{C_2H_4}=4,2\left(g\right)\\ n_{C_2H_4}=\dfrac{4,2}{28}=0,15\left(mol\right)\\ \%V_{C_2H_4}=\dfrac{0,15}{0,35}=42,85\%\\ \%V_{CH_4}=100\%-42,85\%=57,15\%\)

Khi dẫn X qua AgNO3/NH3 thì chỉ có propin phản ứng
CHΞC-CH3 + AgNO3 + NH3 → AgCΞC-CH3 ↓ + NH4NO3
nAgCΞC-CH3 = \(\dfrac{29,4}{147}\)= 0,2 mol = nPropin
Nếu dẫn X qua bình đựng dd brom dư thì khối lượng bình tăng = mPropin + m Etilen
<=> 12,2 = mPropin + m Etilen
<=> 0,2.40 + mEtilen = 12,2
<=> mEtilen = 4,2 gam => nEtilen = 4.2:28 = 0,15 mol
nX = 10,08 : 22,4 = 0,45 mol
=> %V Etilen = \(\dfrac{0,15}{0,45}\).100% = 33,33%
%V Propin = \(\dfrac{0,2}{0,45}\).100% = 44,44%
=> %V Metan = 100 - 33,33 - 44,44 = 22,23%

Ta có: \(n_{Br_2}=\dfrac{6}{160}=0,0375\left(mol\right)\)
PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Theo PT: \(n_{C_2H_4}=n_{Br_2}=0,0375\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,0375.22,4}{6,72}.100\%=12,5\%\\\%V_{CH_4}=87,5\%\end{matrix}\right.\)

- Do dung dịch brom dư, nên khí thoát ra là metan.
![]()
- Chọn đáp án A.

a) \(V_{CH_4}=0,6\left(l\right)\)
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,6}{1,2}.100\%=50\%\\\%V_{C_2H_4}=100\%-50\%=50\%\end{matrix}\right.\)
b) \(n_{C_2H_4}=\dfrac{1,2-0,6}{24}=0,025\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,025-->0,025
=> \(m_{Br_2}=0,025.160=4\left(g\right)\)
c)
\(n_{CH_4}=\dfrac{0,6}{24}=0,025\left(mol\right)\)
=> nH = 0,025.4 = 0,1 (mol)
\(n_{Cl_2}=\dfrac{0,72}{24}=0,03\left(mol\right)\)
=> nCl(thế H) = 0,03 (mol)
Do nH > nCl(thế H)
=> H không bị thế hoàn toàn bởi Cl
=> nHCl = 0,03 (mol)
=> mHCl = 0,03.36,5 = 1,095 (g)
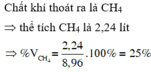
\(n_A=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ n_{Br_2}=\dfrac{40.4\%}{160}=0,01\left(mol\right)\)
PTHH: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,01<---0,01
\(\rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,01}{0,05}.100\%=20\%\\\%V_{CH_4}=100\%-20\%=80\%\end{matrix}\right.\)