Từ 120kg quặng FeS2 ngta sản xuất đc 147kg axit sunfuric. Tính toàn bộ quá trình. Giúp e vs ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C.
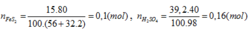
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Từ 120kg FeS2 có thể sản xuất đc bao nhiêu kg axit H2SO4 98%? Biết hiệu suất của cả quá trình là 80%

$n_{FeS_2} = \dfrac{120}{120} = 1(kmol)$
$n_{FeS_2\ pư} = 1.80\% = 0,8(kmol)$
Bảo toàn nguyên tố với S :
$n_{H_2SO_4} = 2n_{FeS_2\ pư} = 1,6(kmol)$
$m_{dd\ H_2SO_4} = \dfrac{1,6.98}{98\%} = 160(kg)$

Khối lượng lưu huỳnh chứa trong 80 tấn quặng:
m S = 80x40/100 = 32 tấn
Điều chế H 2 SO 4 theo sơ đồ sau
S → SO 2 → SO 3 → H 2 SO 4
Ta thấy: Cứ 32g S thì sản xuất được 98g H 2 SO 4
⇒ m H 2 SO 4 = 32x98/32 = 98 tấn
Hiệu ứng phản ứng: H = 73,5/98 x 100 = 75%

Quá trình sản xuất từ \(FeS_2\rightarrow H_2SO_4\)
\(n_{FeS_2}=\dfrac{120}{120}=1\left(mol\right)\\ BTnguyêntố\left(S\right)\Rightarrow n_{FeS_2}.2=n_{H_2SO_4\left(lt\right)}.1\\ \Rightarrow n_{H_2SO_4\left(lt\right)}=2\left(mol\right)\\ \Rightarrow H=\dfrac{m_{H_2SO_4\left(tt\right)}}{m_{H_2SO_4\left(lt\right)}}.100=\dfrac{170}{2.98}.100=86,74\%\)

Đáp án A.
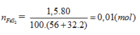
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
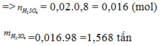

Đề có phải là : ' Từ 80 tấn quặng Pirit chứa 40% lưu huỳnh , người ta sản xuất được 73,5 tấn axit sunfuric . '' đúng không


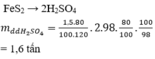

tính toàn bộ hóa trình là sao v=)?