Tính chất hóa học của oxi ,ozon là
A. Chỉ thể hiện tính khử
B. Chỉ thể hiện tính axit
C. Tính khử và tính oxi hóa
D. Chỉ thể hiện tính oxi hóa.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
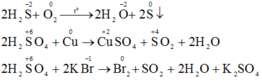

Ba phản ứng trong đó CO thể hiện tính khử:
2CO + O 2 → t ° 2 C O 2
+2 -4
3CO + F e 2 O 3 → t ° 2Fe + 3 C O 2
+2 +4
CO + C l 2 → t ° , x t C O C l 4
+2 +4
Ba phản ứng trong đó có C O 2 thể hiện tính oxi hóa:
C O 2 + C → t ° 2CO
+4 +2
C O 2 + 2Mg → t ° 2MgO + C
+4 0
C O 2 + Zn → t ° ZnO + CO
+4 +2

a)H2S chỉ thể hiện tính khử vì số oxi hóa của S ở mức thấp nhất :-2 .(Không thể giảm nên chỉ có tình khử)
H2SO4 chỉ thể hiện tính oxi hóa vì số oxi hóa của S ở mức cao nhất :6 . (Không thể tăng nên chỉ có tính oxi hóa)
b)H2S + Pb(NO3)2-->PbS + 2HNO3
H2SO4+ FeS -->H2S + FeSO4
C. Tính khử và tính oxi hóa
C. Tính khử và tính oxi hóa