Đun nóng 2,4 gam bột magie với 2,4 gam bột lưu huỳnh trong điều kiện không có không khí, thu được hỗn hợp rắn X. Hòa tan hoàn toàn X vào dung dịch HCl dư, thu được hỗn hợp khí Y. Tỉ khối hơi của Y so với H2 là bao nhiêu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Mg + S → MgS
MgS + 2HCl → MgCl2 + H2S
Mg + 2HCl → MgCl2 + H2
nMg = 0,2 (mol), nS = 0,15 9mol)
nH2S = nMgS = nS = 0,15 mol;
nH2 = nMg (dư) = 0,2 – 0,15 =0,05 (mol)
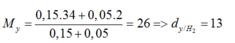

Đáp án C.
Mg + S → MgS
MgS + 2HCl → MgCl2 + H2S
Mg + 2HCl → MgCl2 + H2
nMg = 0,2 (mol); nS = 0,15 (mol)
nH2S = nMgS = nS = 0,15 mol;
nH2= nMg (dư) = 0,2 – 0,15 = 0,05 (mol)
=> MY = (0,15.34+0,05.2)/(0,15+0,05)=26

Đáp án A
F e + S ⇒ M : F e , S , F e S → + H C l F e 2 + X : H 2 S , H 2 ; G : S → + O 2 H 2 O , S O 2
Có 3 chất thay đổi số oxi hóa là Fe, S và Oxi
Bảo toàn e: 4nO2 = 2nFe + 4nSO2 = 2. 0,1 + 4. 0,75= 0,5 mol
=> nO2 = 0,125 mol => V=2,8lít
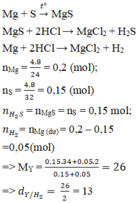
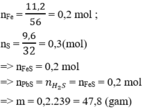
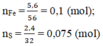
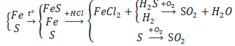

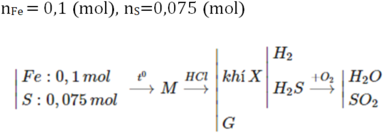

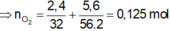
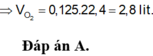
Do hòa tan X vào HCl thu được hỗn hợp lhis
=> Trong X có Mg dư
\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
=> \(n_S=\dfrac{2,4}{32}=0,075\left(mol\right)\)
PTHH: Mg + S --to--> MgS
0,075<-0,075->0,075
Mg + 2HCl --> MgCl2 + H2
0,025---------------->0,025
MgS + 2HCl --> MgCl2 + H2S
0,075------------------->0,075
=> \(M_Y=\dfrac{0,025.2+0,075.34}{0,025+0,075}=26\left(g/mol\right)\)
=> \(d_{Y/H_2}=\dfrac{26}{2}=13\)