Hợp chất hữu cơ A có thành phần khối lượng các nguyên tố như sau:85,7%C và 14,3%H. Biết phân tử khối của A là 28đvC. Công thức hoá học của A là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Vì: %mC+ %mH= 85,7%+14,3%=100%
=> Hợp chất hữu cơ trên chỉ có 2 nguyên tố C và H.
CTTQ: CxHy (x,y: nguyên , dương)
mC= 0,857.28= 24(g) =>x=nC=24/12=2
mH=28-24=4(g) =>y=nH=4/1=4
=> Với x=2;y=4 => Hợp chất hữu cơ A có CTPT: C2H4

Ta có %C + %H + %Cl = 100 %
=> A chứa C , H và Cl
Gọi CTĐGN của A là CxHyClz
=> x:y:z = \(\dfrac{\%C}{12}\): \(\dfrac{\%H}{1}\):\(\dfrac{\%Cl}{35,5}\)= 3,1 : 7,75 : 1,55 = 2 : 5 : 1
=> CTĐGN của A là C2H5Cl và CTPT của A có dạng (C2H5Cl)n
MA = 2,15. 30 = 64,5 (g/mol) => 64,5n = 64,5
=> n = 1 và CTPT của A là C2H5Cl

1. Chất A có dạng C X H Y C l Z
x : y : z = 2,02 : 4,04 : 2,02 = 1 : 2 : 1
Công thức đơn giản nhất là C H 2 C l .
2. MA = 2,25 x 44,0 = 99,0 (g/mol)
( C H 2 C l ) n = 99,0 ⇒ 49,5n = 99,0 ⇒ n = 2
CTPT là C 2 H 4 C l 2 .
3. Các CTCT:
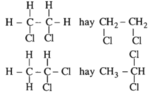

CTDC là : CxHyOz
Khối lượng của các nguyên tố trong hợp chất là :
\(m_C=\frac{M_A\times\%C}{100\%}=\frac{60\times40\%}{100\%}=24\left(g\right)\)
\(m_H=\frac{M_A\times\%H}{100\%}=\frac{60\times6,7\%}{100\%}=4\left(g\right)\)
\(m_O=\frac{M_A\times\%O}{100\%}=\frac{60\times53,3\%}{100\%}=32\left(g\right)\)
Số mol của mỗi nguyên tố trong 1 mol hợp chất là :
\(n_C=\frac{m}{M}=\frac{24}{12}=2\left(mol\right)\)
\(n_H=\frac{m}{M}=\frac{4}{1}=4\left(mol\right)\)
\(n_O=\frac{m}{M}=\frac{32}{16}=2\left(mol\right)\)
Suy ra trong 1 mol hợp chất A có 2 mol C , 4 mol H , 2 mol O
CTT C2H4O2
mC = (60x40):100 = 24 (g)
mH = (6,7x60): 100 = 4 (g)
mO = (53,3x60):100 = 32 (g)
Suy ra:
nC = 24:12 = 2 (mol)
nH = 4:1 = 4 (mol)
nO = 32:2 = 2 (mol)
Vậy CTHH là: C2H4O2

b. Ta có: \(\%_{Na}=100\%-60,68\%=39,32\%\)
Gọi CTĐG của A là: NaxCly
Ta lại có: \(\dfrac{x}{y}=\dfrac{\dfrac{39,32\%}{23}}{\dfrac{60,68\%}{35,5}}\approx\dfrac{1,7}{1,7}=\dfrac{1}{1}\Leftrightarrow\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\)
Gọi CTHH của A là: \(\left(NaCl\right)_n\)
Theo đề, ta có: \(M_{\left(NaCl\right)_n}=\left(23+35,5\right).n=58,5\)(g/mol)
\(\Leftrightarrow n=1\)
Vậy CTHH của A là NaCl
b. Gọi CTĐG của B là: \(Na_aC_bO_c\)
Ta có: \(x:y:z=\dfrac{43,4\%}{23}:\dfrac{11,3\%}{12}:\dfrac{45,3\%}{16}\approx1,9:0,9:2,8\approx2:1:3\)
Gọi CTHH của B là: \(\left(Na_2CO_3\right)_t\)
Theo đề, ta có: \(M_{\left(Na_2CO_3\right)_t}=\left(23.2+12+16.3\right).t=106\)(g/mol)
\(\Leftrightarrow t=1\)
Vậy CTHH của B là Na2CO3

3. Khối lượng mol của hợp chất đó là :
2.28 = 56 (g/mol)
mC = \(\frac{56.85,7}{100}\approx48\left(g\right)\)
mH = 56 - 48 = 8 (g)
nC = \(\frac{48}{12}=4\left(mol\right)\)
nH = \(\frac{8}{1}=8\left(mol\right)\)
Vậy công thức hóa học là C4H8.
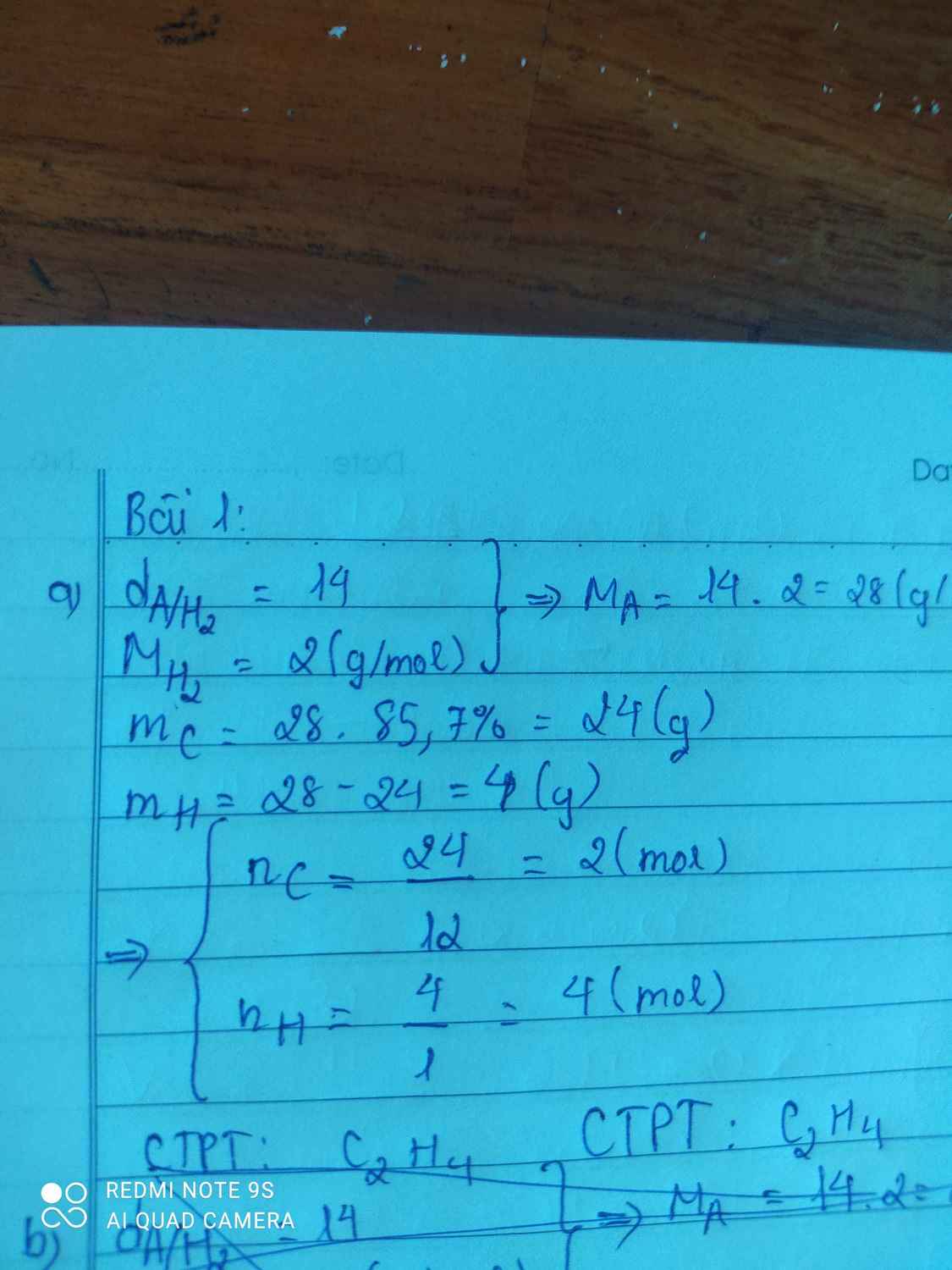
\(\left\{{}\begin{matrix}m_C=85,7\%.28=24g\\m_H=14,3\%.28=4g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}n_C=\dfrac{24}{12}=2mol\\n_H=\dfrac{4}{1}=4mol\end{matrix}\right.\)
\(\Rightarrow CTHH:C_2H_4\)
Vì: %mC+ %mH= 85,7%+14,3%=100%
=> Hợp chất hữu cơ trên chỉ có 2 nguyên tố C và H.
CTTQ: CxHy (x,y: nguyên , dương)
mC= 0,857.28= 24(g) =>x=nC=24/12=2
mH=28-24=4(g) =>y=nH=4/1=4
=> Với x=2;y=4 => Hợp chất hữu cơ A có CTPT: C2H4