Hoà tan 8,6g hỗn hợp Fe & FeCO3 bằng 300g dung dịch HCl 7,3% thu được dung dịch Y và 2,24 dm3 hỗn hợp X gồm 2 khí ở đktc.
a,Tính số gam mỗi chất trong hỗn hợp ban đầu và C% các chấtt trong dung dịch Y
b. Tính dX/H2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Có các phản ứng hóa học xảy ra:
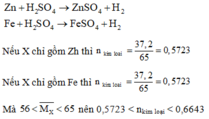
Ta có: n H 2 S O 4 phản ứng = nkim loại < 0,6643
Mà: n H 2 S O 4 ban đầu = 1 > 0,6643 nên sau phản ứng kim loại tan hết, axit còn dư.
b. Khi sử dụng lượng X gấp đôi thì 0,5723.2 < nkim loại < 0,6643.2
Hay 1,1446 < nkim loại < 1,3286
Mà nếu các kim loại bị hòa tan hết thì n H 2 S O 4 phản ứng = nkim loại > 1,1446
Do n H 2 S O 4 thực tế = 1 < 1,1446 nên sau phản ứng kim loại chưa tan hết.
Đán án A

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ \Rightarrow n_{Fe}=0,05\left(mol\right)\\ \Rightarrow m_{Fe}=0,05\cdot56=2,8\left(g\right)\\ \Rightarrow\%_{Fe}=\dfrac{2,8}{6}\cdot100\%\approx46,67\%\\ \Rightarrow\%_{Cu}\approx100\%-46,67\%=53,33\%\)
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05 0,05
\(m_{Fe}=0,05\cdot56=2,8g\)
\(\%m_{Fe}=\dfrac{2,8}{6}\cdot100\%=46,67\%\)

Đáp án D
Fe + 2HCl → FeCl2 + H2
Cr + 2HCl → CrCl2 + H2
nH2 = 1,344: 22,4 = 0,06 mol
- Dựa vào phương trình phản ứng ta có: nFe + nCr = nH2 = 0,06 mol
Và: mhh KL = mFe + mCr => 56nFe + 52nCr = 3,24g
=> nFe = nCr = 0,03 mol
=> mFe = 56.0,03 = 1,68g

So sánh các phản ứng của hỗn hợp X với oxi và hỗn hợp Y với dung dịch HCl, ta thấy :
n HCl = 2 n trong oxit ; m O 2 = 8,7 - 6,7 = 2g
n O trong oxit = 0,125 mol; n HCl = 0,25 mol
V HCl = 0,25/2 = 0,125l
a)
\(n_{HCl}=\dfrac{300.7,3\%}{36,5}=0,6\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
FeCO3 + 2HCl --> FeCl2 + CO2 + H2O
\(n_{khí}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PTHH, nHCl(pư) = 2.nkhí = 0,2 (mol) < 0,6 (mol)
=> HCl dư
Gọi số mol Fe, FeCO3 là a, b (mol)
=> \(\left\{{}\begin{matrix}56a+116b=8,6\\a+b=0,1\end{matrix}\right.\)
=> a = 0,05 (mol); b = 0,05 (mol)
=> \(\left\{{}\begin{matrix}m_{Fe}=0,05.56=2,8\left(g\right)\\m_{FeCO_3}=0,05.116=5,8\left(g\right)\end{matrix}\right.\)
nFeCl2 = 0,1 (mol) => mFeCl2 = 0,1.127 = 12,7 (g)
nHCl(dư) = 0,6 - 0,2 = 0,4 (mol) => mHCl(dư) = 0,4.36,5 = 14,6 (g)
mdd sau pư = 8,6 + 300 - 0,05.2 - 0,05.44 = 306,3 (g)
\(\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{12,7}{306,3}.100\%=4,146\%\\C\%_{HCl\left(dư\right)}=\dfrac{14,6}{306,3}.100\%=4,767\%\end{matrix}\right.\)
b)
\(\overline{M}_X=\dfrac{0,05.2+0,05.44}{0,05+0,05}=23\left(g/mol\right)\)
=> \(d_{X/H_2}=\dfrac{23}{2}=11,5\)