nung nóng chất X xảy ra phản ứng X( rắn )-->Y(rắn ) + Z ( khí ). Sau phản ứng kết thúc thì khỗi lượng chất rắn thu được có thay đổi gì so với chất rắn ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án
Vì khi nung ( C a C O 3 ) , khí C O 2 thoát ra nên khối lượng chất rắn thu được sau phản ứng giảm. Phương trình hóa học :
C a C O 3 → t ° C a O + C O 2

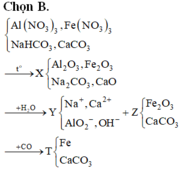
Chọn B.
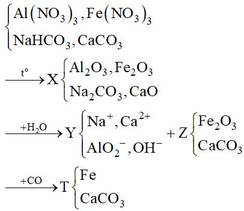
A. Sai, Nhỏ dung dịch HCl vào Y, không có khí thoát ra.
C. Sai, Nhỏ dung dịch HCl vào Y, thất xuất hiện kết tủa trắng sau đó tan nếu dùng HCl dư.
D. Sai, Chất rắn T chứa một đơn chất và một hợp chất

Đáp án C.
Chọn mỗi chất 2 mol
→ Nung nóng hỗn hợp X chứa Al2O3 (1 mol), Na2CO3 (1 mol), Fe2O3 (1 mol), CaO (2 mol)
X + H2O dư → Z chứa CaCO3 (1 mol), Fe2O3 (lmol) → T chứa CaO (1 mol) và Fe (2 mol)

Ban đầu lấy mỗi chất 2 mol → X chứa Al2O3 (1mol), Na2CO3 (1mol), Fe2O3 (1mol), CaO (2mol)
X + H2O dư → Z chứa CaCO3 (1mol), Fe2O3 (1mol)
T chứa CaO (1mol), Fe (2mol)
Đáp án D

Khi nung đá vôi thì tạo ra lượng khí C O 2 đáng kể thoát ra ngoài nên làm khối lượng sản phẩm phản ứng giảm.

a)
$Fe_2(SO_4)_3 + 6KOH \to 2Fe(OH)_3 + 3K_2SO_4$
b)
$n_{Fe_2(SO_4)_3} = 0,3.1 = 0,3(mol)$
$n_{KOH} = \dfrac{16,8}{56} =0,3(mol)$
Ta thấy :
$n_{KOH} : 3 < n_{Fe_2(SO_4)_3} : 1$ nên $Fe_2(SO_4)_3$ dư
$n_{Fe(OH)_3} = \dfrac{1}{3}n_{KOH} = 0,1(mol)$
$n_{Fe_2O_3} = \dfrac{1}{2}n_{Fe(OH)_3} = 0,05(mol)$
$m_{Fe_2O_3} = 0,05.160 = 8(gam)$


Khối lượng chất rắn giảm vì theo định luật bảo toàn khối lượng, ta có:
\(m_X=m_Y+m_Z\)