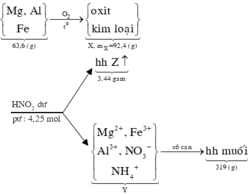
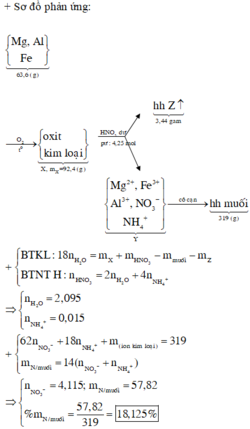
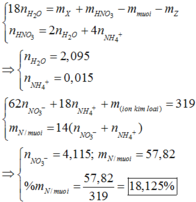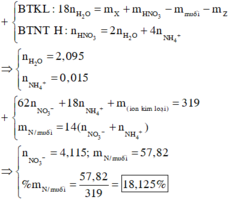Cho khí hiđro dư đi qua 28,8 gam hỗn hợp X gồm R và Oxit kim loại R nung nóng. Sau khi phản ứng xảy ra hoàn toàn thu được 22,4 gam chất rắn. Hòa tan hết lượng chất rắn trên bằng dung dịch HCl thì có 8,96 lít hiđro bay ra ở đktc. a) Xác định kim loại R b) Xác định công thức oxit kim loại R, biết tỉ lệ khối giữa oxit kim loại R và R trong X là 29:7.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


m rắn giảm = mO (oxit) => nO (oxit) = (1,6 – 1,408) : 16 = 0,012mol
Dễ thấy n = nO (oxit) = 0,012mol
=> nH2 ban đầu = 0,012 : 80% = 0,015
=> nFe = nH2= 0,015 → x = 0,015
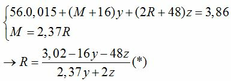
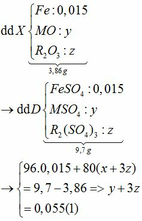
Ta có: CO + O(Oxit) → CO2
Vì: m(Rắn giảm) = mO(Oxit) → nO(Oxit) = (3,86 – 3,46) : 16 = 0,025
TH1: cả 2 oxit đều bị khử bởi CO
→ nO(Oxit) = y + 3z = 0,025 kết hợp với (1) loại
TH2: chỉ có MO bị khử bởi CO
→ nO(Oxit) = nMO = 0,025 → y = 0,025 kết hợp với (1) => z = 0,01
Kết hợp với (*) => M = 64 (Cu)
TH3: chỉ có R2O3 bị khử bởi CO
→ nO(Oxit) = 3.nR2O3 → z = 0,025/3 kết hợp với (1) => y = 0,03
Kết hợp với (*) y => M lẻ => loại
Vậy %m các chất trong X là: 21,76%; 51,81%; 26,43%

2H(Axit) + O(Oxit) → H2O
→ nH(Axit) = 2.nO(Oxit)
Gọi số mol của Fe3O4 và CuO lần lượt là x và y
BTNT O: 4x + y = 0,6
BTKL: 56 . 3x + 64y = 29,6
=> x = 0,1 và y = 0,2
=> %Fe3O4 = 59,18%
%CuO = 40,82%

CuO+H2to→Cu+H2O
Theo PT: nCuO=nCu(1)
Ta có mrắngiảm=mCuO−mCu=3,2(g)
→80nCuO−64nCu=3,2(2)
Từ (1)(2)→nCuO=nCu=\(\dfrac{3,2}{80-64}\)=0,2(mol)(1)(2)
→nCuO=nCu=3,280−64=0,2(mol)
Theo PT: nH2=nCu=0,2(mol)
Đặt hóa trị R là n(n>0)
2R+2nHCl→2RCln+nH2
Theo PT: nR.n=2nH2
→\(\dfrac{13n}{MR}\)=0,4
→MR=32,5n
Với n=2→MR=65(g/mol)
→R là kẽm (Zn)

Chọn đáp án C.
![]()
→ B T K L 92 , 4 + 63 . 4 , 25 = 319 + 3 , 44 + m H 2 O
⇒ n H 2 O = 2 , 095 m o l
→ B T N T H n N H 4 + = 4 , 25 - 2 . 2 , 095 4 = 0 , 015 m o l
⇒ m N O 3 - Y = 255 , 13 g
⇒ n N O 3 - Y = 4 , 115 m o l
⇒ % m N m u ố i = 18 , 125 %