Bài 3: Đốt cháy hoàn toàn 6,72 lít (đktc) một hiđrôcacbon A bằng không khí. Sau phản ứng thu được 26,4 gam CO2 và 5,4 gam nước.
a) Viết phương trình phản ứng
b) Tìm công thức phân tử, viết công thức cấu tạo, gọi tên hiđrôcacbon A.
c) Tính thể tích không khí cần dùng (đktc). Biết không khí đã dùng dư 20% so với lượng phản ứng.

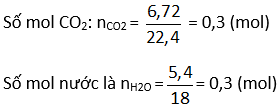
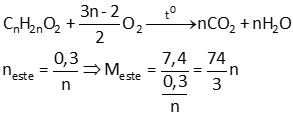
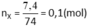
a) 2CxHy + \(\dfrac{4x+y}{2}\)O2 --to--> 2xCO2 + yH2O
b) \(n_A=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
=> nC = 0,6 (mol)
Số nguyên tử C = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
=> nH = 0,6 (mol)
Số nguyên tử H = \(\dfrac{0,6}{0,3}=2\) (nguyên tử)
=> CTPT: C2H2 (axetilen)
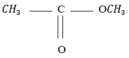
CTCT: \(CH\equiv CH\)
c)
PTHH: 2C2H2 + 5O2 --to--> 4CO2 + 2H2O
0,3--->0,75
=> VO2(lý thuyết) = 0,75.22,4 = 16,8 (l)
=> Vkk(lý thuyết) = 16,8.5 = 84 (l)
=> \(V_{kk\left(thực.tế\right)}=\dfrac{84.120}{100}=100,8\left(l\right)\)