Đốt cháy hòan tòan 448ml một hiđrocacbon A , cần dùng vừa đủ 5,6 lít không khí. Sản phẩm cháy cho vào dd Ba(OH)2 dư thu được 7,88 g kết tủa.(Biết các thể tích khí đều đo ở đktc ,oxi chiếm 20% thể tích không khí ).
a. Xác định công thức phân tử của hidrocacbon A.
b. Cho mg hỗn hợp X gồm chất A và C4H6 (biết d hhX / CH4 là 2,675 )đi qua dung dịch Brom dư sau phản ứng có 32 g brom phản ứng. Mặt khác cũng lượng hỗn hợp X trên khi cho qua dung dịch AgNO3/NH3 dư thu được 19,26 g kết tủa. Tính % thể tích và CTCT của từng chất trong X 

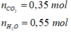

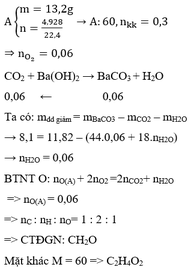
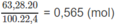
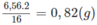
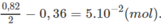
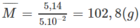
a) \(n_A=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(n_{O_2}=\dfrac{\dfrac{5,6}{22,4}.20}{100}=0,05\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{7,88}{197}=0,04\left(mol\right)\)
=> nC = nCO2 = 0,04 (mol)
Số nguyên tử C = \(\dfrac{0,04}{0,02}=2\) (nguyên tử)
Bảo toàn O: \(n_{H_2O}=0,05.2-0,04.2=0,02\left(mol\right)\)
=> nH = 0,04 (mol)
Số nguyên tử H = \(\dfrac{0,04}{0,02}=2\) (nguyên tử)
=> CTPT: C2H2
b)
Gọi \(\left\{{}\begin{matrix}n_{C_2H_2}=a\left(mol\right)\\n_{C_4H_6}=b\left(mol\right)\end{matrix}\right.\)
\(\overline{M}=\dfrac{26a+54b}{a+b}=2,675.16=42,8\left(g/mol\right)\)
=> \(a=\dfrac{2}{3}b\) (1)
\(\left\{{}\begin{matrix}\%V_{C_2H_2}=\dfrac{a}{a+b}.100\%=\dfrac{\dfrac{2}{3}b}{\dfrac{2}{3}b+b}.100\%=40\%\\\%V_{C_4H_6}=100\%-40\%=60\%\end{matrix}\right.\)
TN1: \(n_{Br_2}=\dfrac{32}{160}=0,2\left(mol\right)\)
PTHH: C2H2 + 2Br2 --> C2H2Br4
a---->2a
C4H6 + 2Br2 --> C4H6Br4
b---->2b
=> 2a + 2b = 0,2 (2)
(1)(2) => a = 0,04 (mol); b = 0,06 (mol)
PTHH: C2H2 + 2AgNO3 + 2NH3 --> C2Ag2 + 2NH4NO3
0,04-------------------------->0,04
C4H6 + AgNO3 + NH3 --> C4H5Ag + NH4NO3
0,06----------------------->0,06
=> mkt = 0,04.240 + 0,06.161 = 19,26 (g)
--> Thỏa mãn đề bài
=> C4H6 có pư với AgNO3/NH3
=> C4H6 là ankin có nối ba đầu mạch
CTCT:
C2H2: \(CH\equiv CH\)
C4H6: \(CH\equiv C-CH_2-CH_3\)