cho hỗn hợp A có khối lượng 2,6g . đốt cháy A thu 1,8g h2o và 8,8g co2 . trong A có nguyên tố nào
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Đốt X thu CO2 và H2O. → X chứa C và H, có thể có O.
Ta có: \(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
⇒ mC + mH = 0,2.12 + 0,6.1 = 3 (g) < 4,6 (g)
→ X gồm: C, H và O.
mO = 4,6 - 3 = 1,6 (g) \(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
- Gọi: CTHH của X là CxHyOz.
\(\Rightarrow x:y:z=0,2:0,6:0,1=2:6:1\)
→ CTĐGN của X là (C2H6O)n.
Mà: \(M_X=23.2=46\left(g/mol\right)\)
\(\Rightarrow n=\dfrac{46}{12.2+6+16}=1\)
Vậy: CTHH của X là C2H6O.

\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
Bảo toàn O: \(n_{O_2}=\dfrac{0,2.2+0,1.1}{2}=0,25\left(mol\right)\)
=> \(V_{O_2}=0,25.22,4=5,6\left(l\right)\)

\(n_{CO_2}=\dfrac{13,2}{44}=0,3mol\Rightarrow n_C=0,3mol\Rightarrow m_C=3,6g\)
\(n_{H_2O}=\dfrac{1,8}{18}=0,1mol\Rightarrow n_H=0,2mol\Rightarrow m_H=0,2g\)
Có \(m_C+m_H=3,8g>m_A=2,8g\Rightarrow\)đề vô lí

Câu 2 :
a)
\(n_{CO_2} = \dfrac{0,3.10^{23}}{6.10^{23}} = 0,05(mol)\\ n_{O_2} = \dfrac{0,9.10^{23}}{6.10^{23}} = 0,15(mol)\)
Vậy :
\(\%n_{CO_2} = \dfrac{0,05}{0,15+0,05}.100\% = 25\%\\ \%n_{O_2} = 100\% - 25\% = 75\%\)
b)
Sục hỗn hợp vào dung dịch Ca(OH)2 lấy dư,thu lấy khí thoát ra ta được O2.Lọc dung dịch,thu lấy kết tủa
\(Ca(OH)_2 + CO_2 \to CaCO_3 + H_2O\)
Cho kết tủa vào dung dịch HCl lấy dư, thu lấy khí thoát ra. Ta thu được khí CO2
\(CaCO_3 + 2HCl \to CaCl_2 + CO_2 + H_2O\)

Đốt cháy A thu được sản phẩm chứa nguyên tố H (H2O)
=> Trong A chứa H
Mà A là hợp chất hữu cơ
=> A chứa C, H
\(n_{H_2O}=\dfrac{1,8}{18}=0,1\left(mol\right)\)
=> nH = 0,2 (mol)
=> \(n_C=\dfrac{2,6-0,2.1}{12}=0,2\left(mol\right)\)
Xét nC : nH = 0,2 : 0,2 = 1 : 1
=> CTPT: (CH)n
Mà MA = 13.2 = 26 (g/mol)
=> n = 2
=> CTPT: C2H2

Đáp án A
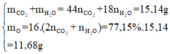
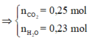
![]()
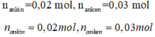
· Đặt CTPT của ankin là CnH2n-2; anken là CmH2m
0,02n + 0,03m = 0,25 2n + 3m = 25
· Do tỉ lệ số mol A, B thay đổi mà số mol CO2 không đổi n = m
Tổng số nguyên tử C trong A và B là 10

Số mol O2=0,3mol
Số mol CO2=0,2mol
Bảo toàn khối lượng
m(H2O)=4,6+0,3.32-8,8=5,4g
Số mol h2o=0,3mol
Bảo toàn ngto O
nO= 2.0,2+0,3-0,3.2=0,1mol
nC:nH:nO=2:6:1
=> công thức C2H6O

\(n_C=n_{CO_2}=\dfrac{8,8}{44}=0,2mol\)
\(n_H=2.n_{H_2O}=2.\dfrac{1,8}{18}=0,2mol\)
\(n_O=\dfrac{2,6-\left(0,2.12+0,2.1\right)}{16}=\dfrac{2,6-2,6}{16}=\dfrac{0}{16}=0\)
Vậy A có nguyên tố là C và H
có phương trình hóa học ko bn