Đốt cháy hoàn toàn 1,82 gam hỗn hợp C4H10, C3H4, C2H2, dẫn toàn bộ sản phẩm vào bình 1 đựng P2O5 dư, bình 2 đựng dung dịch Ca(OH)2 dư. Sau khi phản ứng xong thấy khối lượng bình 1 tăng 2,34 gam, bình 2 có m gam kết tủa. Tìm m.
Giúp em bài này với ạ!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
- Đốt cháy hỗn hợp este thì
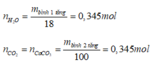
- Nhận thấy rằng
![]()
nên trong X chỉ chứa các este no, đơn chức, mạch hở.

Đáp án D
- Đốt cháy hỗn hợp este thì:
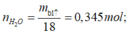
n CO 2 = n CaCO 3 = m b 2 ↑ 100 = 0 , 345
- Nhận thấy rằng n CO 2 = n H 2 O , nên trong X chỉ chứa các este no, đơn chức, mạch hở.

Đáp án : D
Vì là hỗn hợp 2 anken => cháy tạo sản phẩm nCO2 = nH2O
.mII – mI = mCO2 – mH2O = 39g
=> nCO2 = nH2O = 1,5 mol
,nM = 0,4 mol => Số C trung bình = 3,75
=> X là C3H6 và Y là C4H8 với số mol lần lượt là x và y
=> x + y = 0,4 mol ; nCO2 = 3x + 4y = 1,5 mol
=> x = 0,1 mol ; y = 0,3 mol
=> %mY(C4H8) = 80%

Đáp án A
Đốt cháy X tạo CO2 và H2O
Bình 1 giữ lại H2O => mH2O = 7,2g => nH = 2nH2O = 0,8 mol
Bình 2 giữ lại CO2 : nCaCO3 = nCO2 = 0,3 mol
Có : mC + mH + mO = mX => nO = 0,1mol
=> nC : nH : nO = 0,3 : 0,8 : 0,1 = 3 : 8 : 1
Vậy CTĐG nhất của X là C3H8O
Khối lượng \(\left(1\right)\) tăng \(H2O\) sinh ra
\(\Rightarrow n_{H_2O}=\dfrac{2,34}{18}=0,13\)
Sơ đồ phản ứng : \(C_xH_y+O_2\rightarrow CO_2+H_2O\)
Bảo toàn các nguyên tố \(C;H\)
\(m_X=m_C+m_H\Rightarrow n_{CO2}=n_C=\dfrac{m_X-m_H}{12}=\dfrac{1,82-0,13.2}{12}=0,13\)
Bài toán cho ta \(0,13\left(mol\right)CO2\) và \(0,1\left(mol\right)Ca\left(OH\right)_2\)
Ta thấy tạo thành 2 muối :
Giai hệ \(\left\{{}\begin{matrix}n_{HCO_3}+n_{CO_3^2}=n_{CO_2}\\n_{HCO_3}+2n_{CO^2_3}=n_{OH}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{HCO_3}=0,06\\n_{CO^2_3}=0,07\end{matrix}\right.\)
Như vậy sẽ có \(0,07\left(mol\right)CaCO_3\) kết tủa
\(\Rightarrow m\downarrow=0,07.100=7\)
cảm ơn bạn nhiều !!!