hòa tan 6g kim loại m vào hcl dư sau phản ứng kết thúc thấy dung dịch tăng 5,5g. m là kim loại nào
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


mtăng = mM - mH2 = 5.5 (g)
=> mH2 = 6 - 5.5 = 0.5 (g)
nH2 = 0.5/2 = 0.25 (mol)
2M + 2nHCl => 2MCln + nH2
0.5/n.................................0.25
MM = 6/0.5/n = 12n
BL :
n = 2 => M = 24
M là : Mg

`MO + 2HCl -> MCl_2 + H_2O`
Theo PT: `n_(MO) = (n_(HCl))/2`
`<=> 8/(M_M +16) = (0,4)/2`
`<=> M_M = 24`
`=>M` là `Mg`.
\(MO+2HCl\rightarrow MCl_2+H_2O\)
Ta có : \(n_{MO}=\dfrac{1}{2}n_{HCl}=0,2\left(mol\right)\)
=> \(M_{MO}=\dfrac{8}{0,2}=40\)
=> M=24 (Mg)

a) \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,5}{n}\left(mol\right)\)
Ta có : \(M_M=\dfrac{16,25}{\dfrac{0,5}{n}}=32,5n\)
Chạy nghiệm n
n=1 => M=32,5 (loại)
n=2 => M=65 ( chọn)
n=3 => M=97,5 (loại)
Vậy M là Zn
b) Ta có : \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(lít\right)\)

nHCl = 0,35 . 1 = 0,35 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,175 0,35 0,175 0,175 (mol)
nHCl (pứ 2 ) = 0,2 . 2 = 0,4 (mol)
\(X+2HCl\rightarrow XCl_2+H_2\)
0,2 0,4
\(nX=0,175+0,2=0,375\left(mol\right)\)
=> \(MX=\dfrac{11,7}{0,375}=\) 31,2 .-. k ra là s

\(n_{H_2} = \dfrac{4,35-3,95}{2} = 0,2(mol)\\ Mg + 2HCl \to MgCl_2 + H_2\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\)
\(\left\{{}\begin{matrix}Mg:x\left(mol\right)\\Al:y\left(mol\right)\end{matrix}\right.\)→ \(\left\{{}\begin{matrix}24x+27y=4,35\\x+1,5y=0,2\end{matrix}\right.\)→\(\left\{{}\begin{matrix}x=0,125\\y=0,05\end{matrix}\right.\)
Vậy :
\(\%m_{Mg} = \dfrac{0,125.24}{4,35}.100\% = 68,97\%\\ \%m_{Al} = 100\% - 68,97\% = 31,03\%\)

Đáp án C
Số mol H2 thu được là: n H 2 = 0 , 8 2 = 0 , 4 m o l
Gọi n là hóa trị của M
Phương trình hóa học:
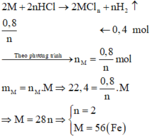
=> M là Fe

\(a/\\ M+2nHCl \to MCl_n+nH_2\\ n_{H_2}=\frac{5,6}{22,4}=0,25(mol)\\ n_M=\frac{1}{n}.n_{H_2}=\frac{1}{n}.0,25=\frac{0,25}{n}(mol)\\ M_M=\frac{16,25.n}{0,25}=65.n(g/mol)\\ \text{Chạy biện luân:}\\ \Rightarrow n=1; R=65(Zn)\\ b/\\ Zn+2HCl\to ZnCl_2+H_2\\ n_{HCl}=2.n_{H_2}=2.0,25=0,5(mol)\\ V_{HCl}=\frac{0,5}{0,2}=2,5M \)
Số mol của khí hidro ở dktc
nH2 = \(\dfrac{V_{H2}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Pt : M + 2HCl → MCl2 + H2\(|\)
1 2 1 1
0,25 0,25
a) Số mol của kim loại M
nM = \(\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
⇒ MM = \(\dfrac{m_M}{n_M}=\dfrac{16,25}{0,25}=65\) (dvc)
Vậy kim loại M là Zn
b) Zn + 2HCl → ZnCl2 + H2\(|\)
1 2 1 1
0,25 0,5
Số mol của dung dịch axit clohidric
nHCl = \(\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
Thể tích của dung dịch axit clohdric cần dùng
CMHCl = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{0,5}{0,2}=2,5\left(M\right)\)
Chúc bạn học tốt
các pro giúp mik
Tham khảo:
Vì sau p/ư khối lượng dung dịch tăng 0,55g và trong quá trình phản ứng có giải phóng khí H2 nên
m\(_{H_2}\)= 6-5,5= 0,5g
=> n\(_{H_2}\)= 0,5:2= 0.25 mol
PTHH: R + 2HCl --> RCl(2) + H(2)
0,25 mol <-- 0,25 mol
=>MR= 6:0,25=24(g/mol)
vậy kl cần tìm là magie (Mg)