Nhúng một thanh sắt nặng 20gam dung dịch CUso4 sau một thời gian lấy thanh sắt ra cân nặng 26,4gam tính khối lượng Cu thoát ra
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


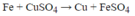
Theo phương trình cứ 56 gam Fe tan vào dung dịch thì có 64 gam Cu tách ra khỏi dung dịch. Thanh Fe tăng khối lượng nên khối lượng dung dịch phải giảm đi đúng bằng khối lượng thanh Fe tăng lên.
Vậy khối lượng thanh sắt tăng 0,8 gam khối lượng dung dịch giảm so với ban đầu 0,8 gam

Cứ 2 mol Al → 3 mol Cu khối lượng tăng 3.64 - 2.27 = 138 g
Theo đề n mol Cu khối lượng tăng 46,38 - 45 = 1,38 g
![]()
Đáp án C

Đáp án B
Bảo toàn ne=> 3nAl = 2nH2=> nAl = 0,1 => %mAl = 0,1.27.100%/5 = 54%

Đáp án : C
2Al + 3Cu2+ -> 2Al3+ + 3Cu
, x -> 1,5x -> 1,5x
=> msau - mtrước = 64.1,5x – 27x = 46,38 – 45
=> x = 0,02 mol => mCu pứ = 1,5.0,02.64 = 1,92g

Chọn C
2Al + 3Cu2+ → 2Al3+ + 3Cu
x → 1,5x
Ta có ∆m = mCu – mAl ⇒ 46,38 – 45 = 64.1,5x – 27x ⇒ x = 0,02
⇒ mCu = 64.1,5.0,02 = 1,92g

Khối lượng thanh sắt tăng: 50x4/100 = 2(g). Gọi khối lượng sắt tác dụng là x gam
Phương trình hóa học của phản ứng:
Fe + CuSO 4 → FeSO 4 + Cu
Theo phương trình hóa học trên và đề bài, ta có:
64x/56 - x = 2
=> x= 14g; n Fe = 14/56 = 0,25 mol
Vậy khố lượng Cu sinh ra là 16 gam
Fe + CuSO 4 → FeSO 4 + Cu
n FeSO 4 = n Fe = 0,25
C M FeSO 4 = 0,25/0,5 = 0,5M
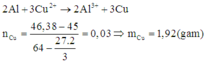
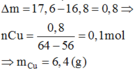
$PTHH:Fe+CuSO_4\to FeSO_4+Cu\downarrow$
Đặt $n_{Cu}=x(mol)\Rightarrow n_{Fe}=x(mol)$
$m_{KL tăng}=m_{Cu}-m_{Fe}=26,4-20$
$\Rightarrow 64x-56x=6,4$
$\Rightarrow x=0,8$
$\Rightarrow m_{Cu}=0,8.64=51,2(g)$