Cho 2,3g kim loại kiềm R tác dụng với lượng nước dư thu được dung dịch A và V lít khí (đktc). Trung hoà dung dịch A cần 100ml HCl 1M a) Xác định tên R b) Tính V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(\text{Đ}\text{ặt}:A\\ A+HCl\rightarrow ACl+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_A=n_{ACl_2}=2.n_{H_2}=0,1.2=0,2\left(mol\right)\\ M_{ACl}=\dfrac{11,7}{0,2}=58,5\left(\dfrac{g}{mol}\right)\\ M\text{à}:M_{ACl}=M_A+35,5\\ \Rightarrow M_A=23\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Natri\left(Na\right)\\ a=23.0,2=4,6\left(g\right)\)
nH2=2,24/22,4=0,1(mol)
2M+2HCl→2MCl+H2
0,2 ← 0,2 ← 0,1
Có 0,2 .(M+35,5)=11,7(gam)
⇒ M=23 ⇒M là Na
mNa=23. 0,2= 4,6 (gam)

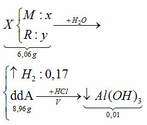
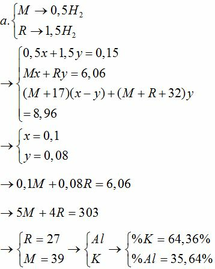
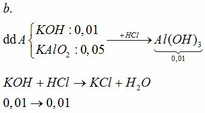
TH1: kết tủa Al(OH)3 chưa bị hòa tan
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,01 ←0,01
→ nHCl = 0,02
→ V = 0,02 (lít) = 20 (ml)
TH2: kết tủa Al(OH)3 bị hòa tan một phần
KAlO2 + HCl +H2O → KCl + Al(OH)3↓
0,05 → 0,05 0,05
Al(OH)3 + 3HCl → AlCl3 + 3H2O
0,04` → 0,12
→ nHCl = 0,18 → V = 0,18 (l) = 180 (ml)
Vậy có 2 giá trị của V thỏa mãn là: 20 ml và 180 ml

a. PTHH: R + H2SO4 ---> RSO4 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
Theo PT(1): \(n_R=n_{H_2}=0,16\left(mol\right)\)
=> \(M_R=\dfrac{3,84}{0,16}=24\left(g\right)\)
Vậy R là magie (Mg)
b. PTHH:
Mg + HCl ---> MgCl2 + H2 (2)
Theo PT(2): \(n_{H_2}=n_{Mg}=0,16\left(mol\right)\)
=> \(V_{H_2}=0,16.22,4=3,584\left(lít\right)\)
(Do câu b đề ko rõ lắm nên mik làm như vậy, nếu sai bn bình luận nhé.)

a) \(n_{H_2}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
2A + 2HCl --> 2ACl + H2
2B + 2HCl --> 2BCl2 + H2
=> nA + nB = 2.nH2 = 0,16
=> \(\overline{M}_{hh}=\dfrac{4,8}{0,16}=30\)
Mà A, B thuộc 2 chu kì liên tiếp nhóm IA
=> A, B là Na, K
b)
Gọi số mol Na, K là a,b
=> 23a + 39b = 4,8
2Na + 2HCl --> 2NaCl + H2
_a----->a-------------->0,5a
2K + 2HCl --> 2KCl + H2
_b--->b-------------->0,5b
=> 0,5a + 0,5b = 0,08
=> a = 0,09; b = 0,07
nHCl(PTHH) = a + b = 0,16
=> nHCl(thực tế) = 0,16.125% = 0,2(mol)
=> \(V_{ddHCl}=\dfrac{0,2}{1}=0,2\left(l\right)\)

Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe

\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(R+2HCl\rightarrow RCl_2+H_2\)
\(0.1........0.2................0.1\)
\(M_R=\dfrac{13.7}{0.1}=137\left(\dfrac{g}{mol}\right)\)
\(R:Ba\)
\(200\left(ml\right)=0.2\left(l\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)

nMg = 0,1(mol)
PTHH: Mg + 2HCl --> MgCl2 +H2
nMg = nMgCl2= nH2 = 0,1(mol)
=> mmuối = 9,5(g)
VH2 = 2,24(l)
b) CMHCl = 0,2/0,1=2(M)


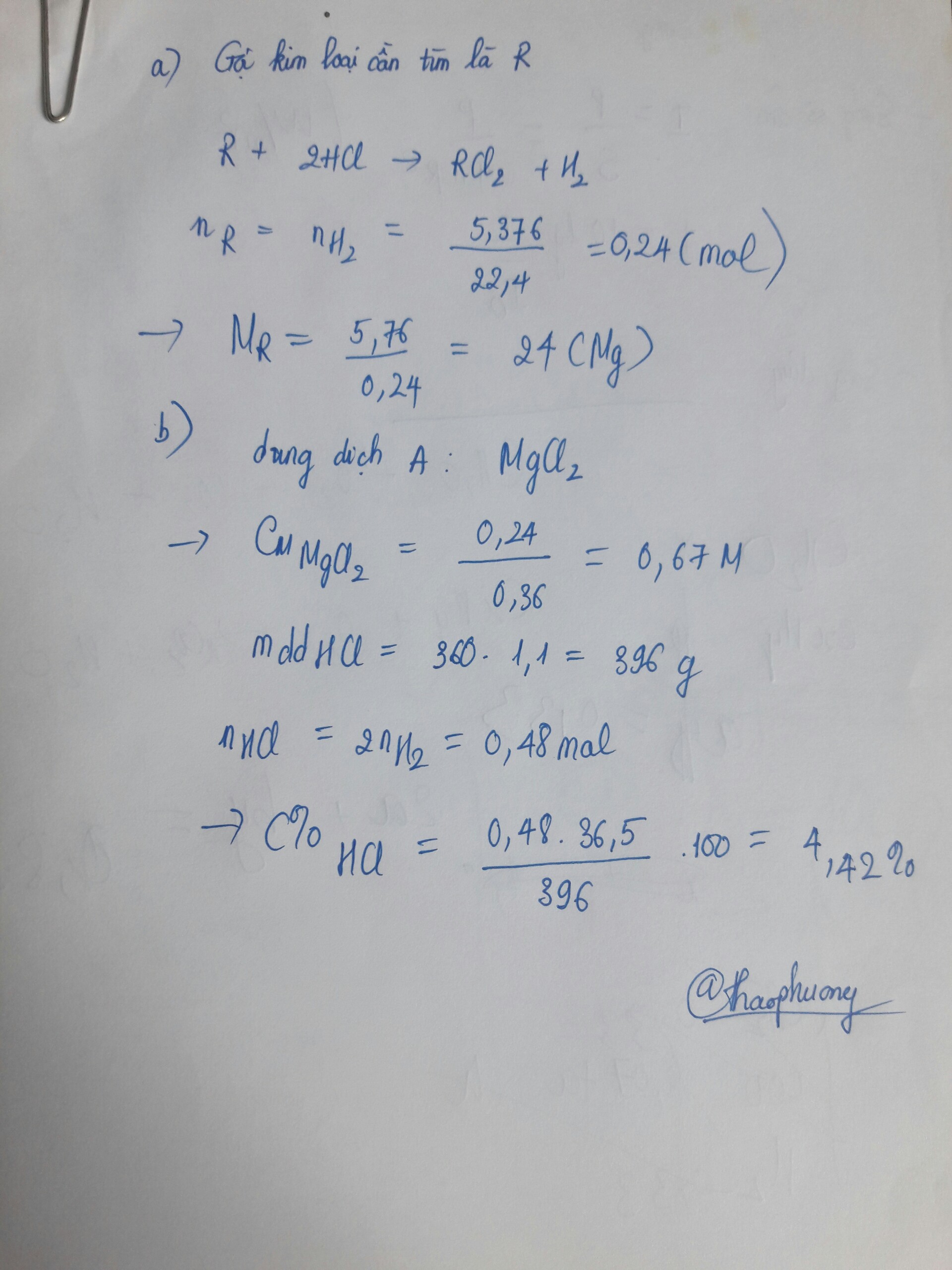
a) nHCl = 0,1.1 = 0,1 (mol)
PTHH: 2R + 2H2O --> 2ROH + H2
0,1<---------------0,1---->0,05
ROH + HCl --> RCl + H2O
0,1<--0,1
=> \(M_R=\dfrac{2,3}{0,1}=23\left(g/mol\right)\)
=> R là Na
b) VH2 = 0,05.22,4 = 1,12(l)