Cho 2,24 g sắt tác dụng với dd HCl dư.Khí sinh ra cho đi qua ống đựng 4,2 g CuO được đốt nóng.Xác định khối lượng của chất rắn ở trong ống sau khi phản ứng xảy ra hoàn toàn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Fe + 2HCl → Fe Cl 2 + H 2 (1)
Theo PTHH (1) ta có
n H 2 = n Fe = 2,24/56 = 0,04 mol
CuO + H 2 → Cu + H 2 O (2)
Theo PTHH (2) :
Số mol CuO phản ứng : n CuO = n H 2 = 0,04 mol.
Số mol Cu tạo ra là 0,04 mol.
Số mol CuO dư 4,2/80 - 0,04 = 0,0125 mol
Sau phản ứng trong ống nghiệm có: m Cu = 64 x 0,04 = 2,56g
m CuO = 80 x 0,0125 = 1g
Khối lượng chất rắn : 1+ 2,56=3,56 (g).

Fe+2HCl--->FeCl2+H2
H2+CuO-->Cu+Fe
Ta có
n Fe=2,24/56=0,04(mol)
Theo pthh1
n H2=n Fe=0,04(mol)
n CuO=4,2/80=0,0525(mol)
--->CuO dư
n CuO dư=0,0525-0,04=0,0125(mol)
m CuO=0,0125.80=1(g)
n Cu=n H2=0,04(mol)
m Cu=0,04.64=2,56(g)
m chất rắn =1+2,56=3,56(g)

Theo gt ta có: $n_{CO}=0,1(mol)$
Bảo toàn nguyên tố C và theo tỉ khối ta có:
$n_{CO}=0,025(mol);n_{CO_2}=0,075(mol)$
Ta lại có: $n_{O/oxit}=n_{CO_2}=0,075(mol)$
Gọi CTTQ của oxit sắt đó là $Fe_xO_y$
Ta có: $M_{Fe_xO_y}=\frac{160y}{3}$
Do đó công thức của oxit sắt là $Fe_3O_4$

a.b.
\(n_{Fe}=\dfrac{8,4}{56}=0,15mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,15 0,15 ( mol )
\(V_{H_2}=0,15.22,4=3,36l\)
c.\(n_{CuO}=\dfrac{9,6}{80}=0,12mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,12 < 0,15 ( mol )
0,12 0,12 ( mol )
\(m_{Cu}=0,12.64=7,68g\)

\(n_{Na}=\dfrac{1,84}{23}=0,08\left(mol\right);n_{CuO}=\dfrac{3,2}{80}=0,04\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,08 0,04
PTHH: H2 + CuO → Cu + H2O
Mol: 0,02 0,02 0,02
Ta có: \(\dfrac{0,02}{1}< \dfrac{0,04}{1}\) ⇒ H2 hết, CuO dư
\(m_{Cu}=0,02.64=1,28\left(g\right)\)
\(m_{CuOdư}=\left(0,04-0,02\right).80=1,6\left(g\right)\)
\(\Rightarrow m_{chấtrắn}=1,28+1,6=2,88\left(g\right)\)

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

2KMnO4--->MnO2+O2+K2MnO4 (1)
theo bài ra ta có
nKMnO4= \(\frac{79}{158}=0,5\)(mol)
hỗn hợp chất rắn A gồm MnO2 và K2MnO4
theo phương trình (1) ta có
nMnO2= \(\frac{1}{2}x0,5\)= 0,25 (mol)
---> mMnO2= 0.25 x 87=21,75 (g)
nK2MnO4= \(\frac{1}{2}x0,5\)= 0,25 (mol)
----> m K2MnO4= 0,25 x 197=49,25 (g)
--->mA= 21,75+49,25=71 (g)
---> H%= \(\frac{71}{74,2}x100\%\approx95,69\%\)
2)
2) K2MnO4+8 HCl đặc----> 2Cl2+4H2O+2KCl+MnCl2 (2)
MnO2+4 HCl đặc ---> MnCl2 +Cl2+2 H2O (3)
khí thu được là Cl2
Cl2+ Cu-->CuCl2 (4)
3Cl2+2 Fe---> 2FeCl3 (5)
gọi số mol CuCl2 là x (x>0 ;mol)
--> mCucl2= 135x (g)
gọi số mol FeCl3 là y (y>0 ;mol)
---> n FeCl3=162,5 (g)
theo bài ra ta có 135x+162,5y=75,75( ** )
theo phương trình (4) ta có
nCu= nCuCl2=x(mol)
--> mCu= 64x (g)
theo phương trình (5) ta có
nFe=nFeCl3=y (mol )
--> mFe=56y (g)
theo bài ra ta có
64x+56y= 29,6 ( ** )
từ ( * ) và ( ** ) ta có hệ phương trình
\(\hept{\begin{cases}135x+162,5y=75,75\\64x+56y=29,6\end{cases}}\)
=> \(\hept{\begin{cases}x=0,2\\y=0,3\end{cases}}\)
=> mCuCl2= 0,2 x 135=27(g)
mFeCl3= 0,3 x 162,5= 48,75 (g)
LƯU Ý: bạn ghi ngoặc ở phép tính cuối và bạn tự giải phương trình hoặc liên hệ với mình

Đáp án B
X gồm ROH và CH3CH2CH2OH, (CH3)2CHOH.
Có ![]()
Mà CH3CH2CH2OH và (CH3)2CHOH có M = 60 > 46 nên ROH là CH3OH
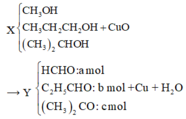
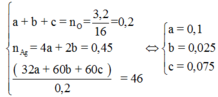
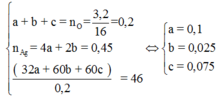

này cái thằng kia muốn gây sự hả mà tự nhiên đi quá người ta
ừ ý
MN đã lm j bn đou