Để điều chế được m kg H3PO4 người ta dùng 3,2 kg photpho a) Viết các phương trình phản ứng xảy ra b) Xác định giá trị m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Al + 6HCl --> 2AlCl3 + 3H2
Fe + 2HCl --> FeCl2 + H2
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
Fe + H2SO4 --> FeSO4 + H2

CaCO3 ---------to------> CaO + CO2
100.................................56.........44 (g)
m<----------------------------280 (g)
=> m=\(\dfrac{280.100}{56}=500\left(g\right)\)
Vì H=80%
=> \(m=\dfrac{500}{80\%}=625\left(g\right)=0,625\left(kg\right)\)
\(n_{CaO}=\dfrac{280}{56}=5\left(mol\right)\)
PTHH: CaO + CO2 → CaCO3
Mol: 5 5
\(\Rightarrow m=m_{CaCO_3}=5.100.80\%=400\left(g\right)=0,4\left(kg\right)\)

a) \(C+O_2-^{t^o}\rightarrow CO_2\)
b) Do sau phản ứng thấy còn dư 49kg than chưa cháy
=> \(m_{C\left(pứ\right)}=490-49=441\left(kg\right)\)
=> \(H=\dfrac{441}{490}.100=90\%\)

a, \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
b, \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{Fe_3O_4}=\dfrac{17,4}{232}=0,075\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,075}{1}>\dfrac{0,2}{4}\), ta được Fe3O4 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Fe_3O_4\left(pư\right)}=\dfrac{1}{4}n_{H_2}=0,05\left(mol\right)\\n_{Fe}=\dfrac{3}{4}n_{H_2}=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe_3O_4\left(dư\right)}=0,075-0,05=0,025\left(mol\right)\)
\(\Rightarrow m_{Fe_3O_4\left(dư\right)}+m_{Fe}=0,025.232+0,15.56=14,2\left(g\right)\)
Số mol của khí H2;
nH2 = \(\dfrac{V}{22.4}\) = \(\dfrac{4.48}{22.4}\) = 0.2 mol
Số mol của 17,4g Fe3O4:
nFe3O4 = \(\dfrac{m}{M}\) = \(\dfrac{17.4}{232}\) = 0,075 mol
PTHH: 2H2 + Fe3O4 \(\rightarrow\) 3Fe + 4H2O
Tỉ lệ : 2 : 1 : 3 : 4
Mol: 0,2 0.075 \(\rightarrow\) 0.225
b.Khối lượng của Fe là
mFe = n.M = 0.225 . 56 = 12.6G

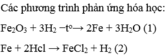

a,b/
pthh:
P + 5HNO\(_3\) → H\(_3\)PO\(_4\)+ 5NO\(_2\) + H\(_2\)O
nP=\(\dfrac{3,2}{31}=0,1kmol\)
P + 5HNO\(_3\) → H\(_3\)PO\(_4\)+ 5NO\(_2\) + H\(_2\)O
0,1--->0,5--------->0,1---->0,5------>0,1
\(mH_3PO_4=0,1.98=9,8kg\)
vậy giá trị m = 9,8 kg