Phân đạm ure có công thức hóa học là CO(NH2)2. Hãy xác định:
a. Khối lượng mol của phân ure.
b. Tính thành phần phần trăm (theo khối lượng) của các nguyên tố N có trong phân.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Thành phần % các nguyên tố trong ure:
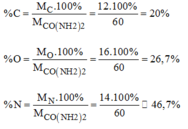
%H = 100-(%C + %O + %N) = 100- ( 20 + 26,7 + 46,7) = 6,6%

a) \(M_{\left(NH_2\right)_2CO}=\left(14.1+1.2\right).2+12.1+16.1=60\left(g/mol\right)\)
b) \(\left\{{}\begin{matrix}\%N=\dfrac{2.14}{60}.100\%=46,67\%\\\%H=\dfrac{1.4}{60}.100\%=6,67\%\\\%C=\dfrac{12.1}{60}.100\%=20\%\\\%O=100\%-46,67\%-6,67\%-20\%=26,66\%\end{matrix}\right.\)

\(a.\%m_N=\dfrac{14.2}{\left(14+4.1\right).2+32+4.16}.100\approx21,212\%\\ \%m_H=\dfrac{4.2}{\left(14+4.1\right).2+32+4.16}.100\approx6,061\%\\ \%m_S=\dfrac{32}{\left(14+4.1\right).2+32+4.16}.100\approx24,242\%\\ \%m_O=\dfrac{4.16}{\left(14+4.1\right).2+32+4.16}.100\approx48,485\%\)
\(b.m_{N\left(20kg\right)}=20.\dfrac{2.14}{\left(14+4.1\right).2+32+4.16}.100\%\approx4,2424\left(kg\right)\)

Câu 2:
Trong 1 mol X: \(\left\{{}\begin{matrix}n_{Ag}=\dfrac{170.63,53\%}{108}=1\left(mol\right)\\n_N=\dfrac{170.8,23\%}{14}=1\left(mol\right)\\n_O=\dfrac{170\left(100\%-63,53\%-8,23\%\right)}{16}=3\left(mol\right)\end{matrix}\right.\)
Vậy CTHH của X là \(AgNO_3\)
Câu 1:
\(a,\%_{Fe}=\dfrac{56}{180}\cdot100\%=31,11\%\\ \%_N=\dfrac{14\cdot2}{180}\cdot10\%=15,56\%\\ \%_O=100\%-31,11\%-15,56\%=53,33\%\\ b,\%_{N\left(N_2O\right)}=\dfrac{14\cdot2}{44}\cdot100\%=63,63\%\\ \%_{O\left(N_2O\right)}=100\%-63,63\%=36,37\%\\ \%_{N\left(NO\right)}=\dfrac{14}{30}\cdot100\%=46,67\%\\ \%_{O\left(NO\right)}=100\%-46,67\%=53,33\%\\ \%_{O\left(NO_2\right)}=\dfrac{16\cdot2}{46}\cdot100\%=69,57\%\\ \%_{N\left(NO_2\right)}=100\%-69,57\%=30,43\%\)

\(m_{Fe}=180.31,11\%=56\left(g\right)\\ m_N=180.15,56\%=28\left(g\right)\\ m_O=180-56-28=96\left(g\right)\)
\(n_{Fe}=\dfrac{56}{56}=1\left(mol\right)\\ n_N=\dfrac{28}{14}=2\left(mol\right)\\ n_O=\dfrac{96}{16}=6\left(mol\right)\)
\(CTHH:Fe\left(NO_3\right)_2\)
(đề lỗi nên mik sửa Bari thành Sắt nhé chứ Bari nặng tới 137 g/mol)

Gọi CTHH là CaxCyOz
Trong hợp chất: mCa = 100.40% = 40 (g) => x = 1
mC = 100.12% = 12 => y = 1
mO =100.48% = 48 => z = 3
=> Hợp chất là CaCO3

`#3107.101107`
a. Sửa đề: Hãy cho biết khối lượng nguyên tử của mỗi nguyên tố có trong phân tử đó.
- Trong phân tử \(\text{SO}_2\) gồm 2 nguyên tử, nguyên tử S và O
`=>` NTK của S là `32` amu, NTK của phân tử O là `16` amu
b.
Khối lượng phân tử của SO2 là:
\(32+16\cdot2=64\left(\text{amu}\right)\)
c.
Số `%` của S có trong SO2 là:
\(\text{%S }=\dfrac{32\cdot100}{64}=50\left(\%\right)\)
Số `%` của O2 có trong SO2 là:
\(\text{%O = 100%}-\text{50% = 50%}\)
Vậy:
a. S: `32` amu, O: `16` amu
b. PTK của SO2 là `64` amu
c. \(\text{%S = 50%; %O = 50%.}\)
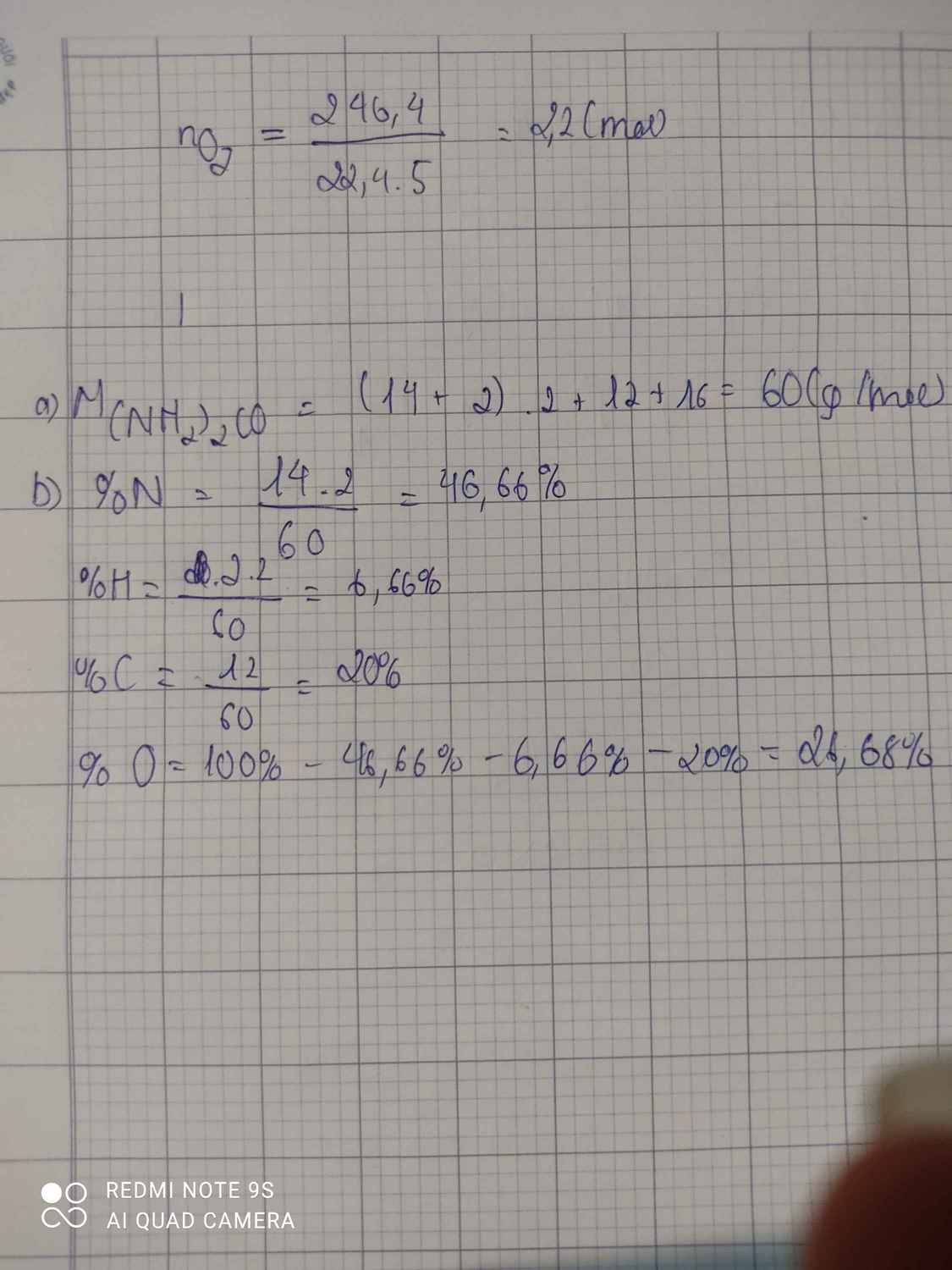
a, 60(g/mol)
b,phần trăm khối lượng N là: 14:(12+16+(14+2).2).100%= 23,3%