Trong công thức H 2 O thì nguyên tố oxi chiếm bao nhiêu phần trăm (%)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Công thức hoá học các hợp chất với oxi và hiđro là CO 2 và CH 4

Gọi công thức phân tử của chất A là CxHyOz
Giả sử z = l thì A là 
Khi đó  (thỏa mãn vì CTPT trùng với CTĐGN)
(thỏa mãn vì CTPT trùng với CTĐGN)
Giả sử z = 2 thì A là 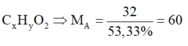
Khi đó 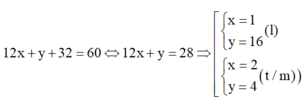
=> C2H4O2 (loại vì công thức đơn giản nhất là CH2O)
Tương tự ta được C3H6O3; C4H8O4;... đều không thỏa mãn
=> Chất A thỏa mãn công thức phân tử cũng là công thức đơn giản nhất chỉ có CH2O.
Vậy tổng số nguyên tử trong A là 4.
Đáp án B

a. Gọi CTHH của A là: X2Oa
Theo đề, ta có: \(d_{\dfrac{A}{H_2O}}=\dfrac{M_A}{M_{H_2O}}=\dfrac{M_A}{18}=6\left(lần\right)\)
=> MA = 108(g)
Theo đề, ta lại có:
\(\%_{X_{\left(A\right)}}=\dfrac{2M_X}{108}.100\%=100\%-74,1\%=25,9\%\)
=> \(M_X\approx14\left(g\right)\)
=> X là nitơ (N)
Ta lại có: \(PTK_A=14.2+16.a=108\left(đvC\right)\)
=> a = 5
b. CTHH của A là: N2O5
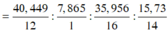

\(\%H=\dfrac{1.2}{18}.100\%=11,1\%\)
\(\%O=\dfrac{16.1}{18}.100\%=88,8\%\)