Hòa tan 0,81 gam bột Al trong dung dịch HNO3 đăc nóng sau phản ứng thu được V lit khí NO2 (ở đktc và là sp khử duy nhất ) Gía trị V là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Ta có: nA1 = 0,03 (mol)
Các phương trình phản ứng:
2Al + Fe2O3 → Al2O3 + 2Fe (1)
2Al + 3CuO → Al2O3 + 3Cu (2)
Gọi số mol Al tham gia phản ứng (1) là x, tham gia phản ứng (2) là y.
Theo (1): nFe = nAl = x (mol)
Theo (2): nCu = 3 2 nAl = 3 2 y (mol)
Fe + 4HNO3loãng → Fe(NO3)3 + NO + 2H2O (3)
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O (4)
Theo (3): nNO/( 3) = nFe = x (mol).
Theo (4): nNO/(4) = 2 3 nCu = 2 3 . 3 2 y = y(mol)
⇒ nNO = x + y = 0,03 (mol) ⇒VNO = 0,03 x 22,4 = 0,672 (lit).

Đáp án D:
Tóm tắt theo sơ đồ:
rFeoOo t° _ Hòa tan hoàn toàn bằng HNO3

Như vậy, thực chất trong bài toán này chỉ có quá trình cho và nhận electron của nguyên tử Al và N.
Các quá trình nhường và nhận electron như sau:
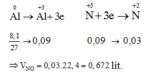

Fe+6HNO3- -->Fe(NO3)3 + 3NO2 + 3H2O
x 6x 3x
mdds=mddt+mFe-mNO2
(126-63*6x)=0.3692*(200+56x-3x*46)
=>x==0.15=>nNO2=0.45=>V=nRT/p=9.89l
nHNO3 = 63%x200/63 = 2 mol
Do acid dư nên Fe --> Fe3+
Gọi m là khối lượng Fe: --> nFe = m/56
2H+ + NO3- + 1 e --> NO2 + H2O
số mol e nhường = số e nhận
--> 3m/56 = nNO2
--> Cứ 2 mol acid tham gia phản ứng thì có 1 mol NO3- của acid tham gia tạo muối và 1 mol tạo khí NO2.
--> lượng acid phản ứng là 3m/56 x 2 = 3m/28
--> (2 - 3m/28)x63/( m+ 200 - 46x3m/56) = 0.3692
-->m = 8.4
--> số mol NO2 là 0.45
n = pV/RT = 1,12xV/0.082x(27+273) = 0.45 --> V = 9.8839(l)\(\approx\)9,89 (l)

Đáp án A
Quy đổi hỗn hợp X gồm Fe và O
mX = 56nFe + 16nO = 10,44 (1)

\(n_{Al}=0,03\left(mol\right)\)
Bảo toàn e:
\(n_{NO_2}=3n_{Al}=0,09\left(mol\right)\)
\(\Rightarrow V=2,016\left(l\right)\)