Cho 13 gam Kẽm Zn tác dụng vừa đủ với 100 gam dung dịch HCl.
a) Viết phương trình hóa học của phản ứng.
b) Tính nồng độ phần trăm dung dịch HCl đã dùng.
c) Tính nồng độ phần trăm dung dịch muối tạo thành.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
b) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(C_{ddHCl}=\dfrac{14,6.100}{100}=14,6\)0/0
c) \(n_{ZnCl2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(m_{ddspu}=13+100-\left(0,2.2\right)=112,6\left(g\right)\)
\(C_{ZnCl2}=\dfrac{27,2.100}{112,6}=24,16\)0/0
Chúc bạn học tốt
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2........0.4..........0.2.......0.2\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(C\%_{HCl}=\dfrac{14.6}{100}\cdot100\%=14.6\%\)
\(m_{ZnCl_2}=0.2\cdot136=27.2\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=13+100-0.2\cdot2=112.6\left(g\right)\)
\(C\%_{ZnCl_2}=\dfrac{27.2}{112.6}\cdot100\%=24.1\%\)

`a)PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,2` `0,4` `0,2` `0,2` `(mol)`
`n_[Zn]=13/65=0,2(mol)`
`b)V_[H_2]=0,2.22,4=4,48(l)`
`c)m_[dd HCl]=[0,4.36,5]/5 . 100=292(g)`
`=>C%_[ZnCl_2]=[0,2.136]/[13+292-0,2.2].100~~8,93%`

nZn=0,1 mol
Zn +2HCl=> ZnCl2+ H2
0,1 mol =>0,2 mol
=>mHCl=36,5.0,2=7,3g
=>m dd HCl=7,3/14,6%=50g
mdd sau pứ=6,5+50-0,1.2=56,3g
=>C% dd ZnCl2=(0,1.136)/56,3.100%=24,16%
a.b. Zn + 2HCl ---> ZnCl2 + H2 (1)
Theo pt: 65g 73g 136g 2g
Theo đề: 6,5g 7,3g 13,6g
=> mddHCl=\(\frac{7,3.100}{14,6}=50\left(g\right)\)
c. Từ pt (1), ta có: \(C_{\%}=\frac{13,6}{50+6,5}.100\%=24,1\%\)
![]()

a) 2NaOH + H2SO4 -- Na2SO4 + 2H2O
b) \(n_{NaOH}=\dfrac{100.20}{100.40}=0,5\left(mol\right)\)
PTHH: 2NaOH + H2SO4 -- Na2SO4 + 2H2O
______0,5----->0,25------>0,25
=> mH2SO4 = 0,25.98 = 24,5 (g)
=> \(m_{ddH_2SO_4}=\dfrac{24,5.100}{19,6}=125\left(g\right)\)
c) mNa2SO4 = 0,25.142 = 35,5 (g)
mdd sau pư = 100 + 125 = 225 (g)
=> \(C\%\left(Na_2SO_4\right)=\dfrac{35,5}{225}.100\%=15,778\%\)

\(a.MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(b.n_{MgO}=\dfrac{16}{40}=0,04mol\)
\(\rightarrow n_{HCl}=0,04.2=0,08mol\)
\(C_{M_{HCl}}=\dfrac{0,08}{0,15}=0,53M\)
\(c.m_{MgCl_2}=0,04.95=3,8g\)

a) $n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{HCl} =2 n_{Fe} = 0,2.2 = 0,4(mol)$
$C\%_{HCl} = \dfrac{0,4.36,5}{200}.100\% = 7,3\%$
b) $n_{H_2} = n_{FeCl_2} = n_{Fe} = 0,2(mol)
Sau phản ứng, $m_{dd} = 11,2 + 200 - 0,2.2 = 210,8(gam)$
$C\%_{FeCl_2} = \dfrac{0,2.127}{210,8}.100\% = 12,05\%$

\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,4 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\
C\%_{HCl}=\dfrac{0,4.36,5}{200}.100\%=7,3\%\)

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}=0,2\left(mol\right)\Rightarrow C\%_{HCl}=\dfrac{0,2.36,5}{400}.100\%=1,825\%\)
c, Theo PT: \(n_{MgCl_2}=n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 2,4 + 400 - 0,1.2 = 402,2 (g)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{0,1.95}{402,2}.100\%\approx2,36\%\)
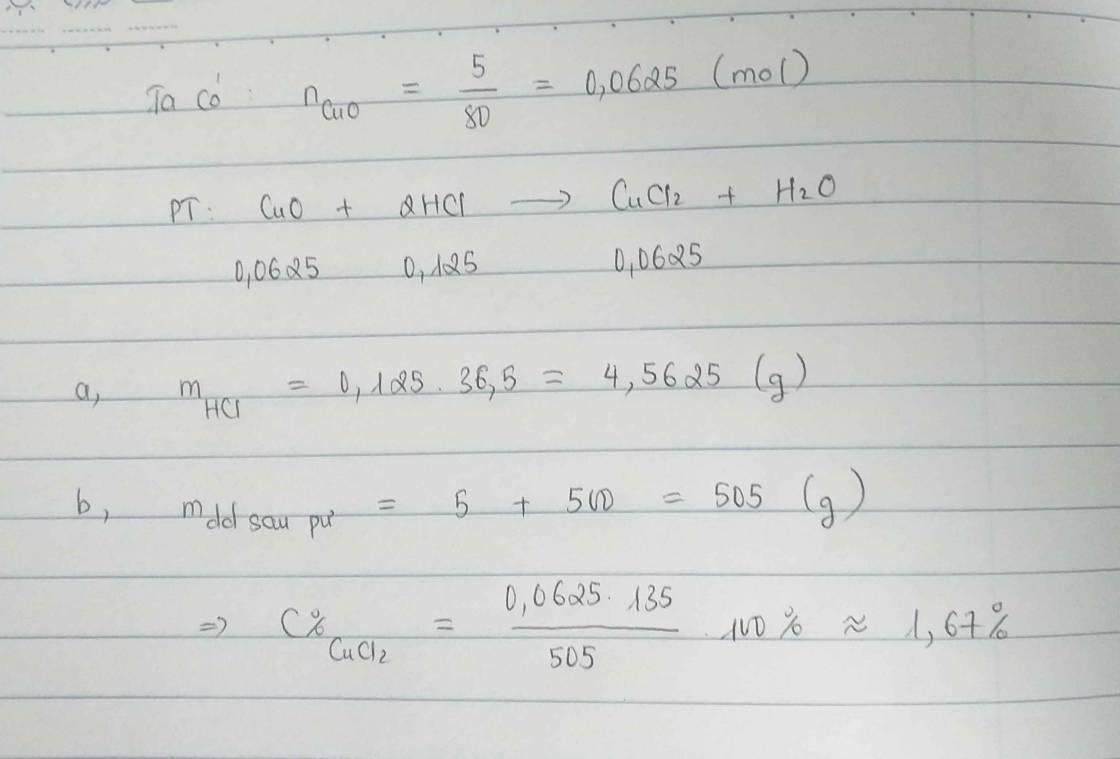
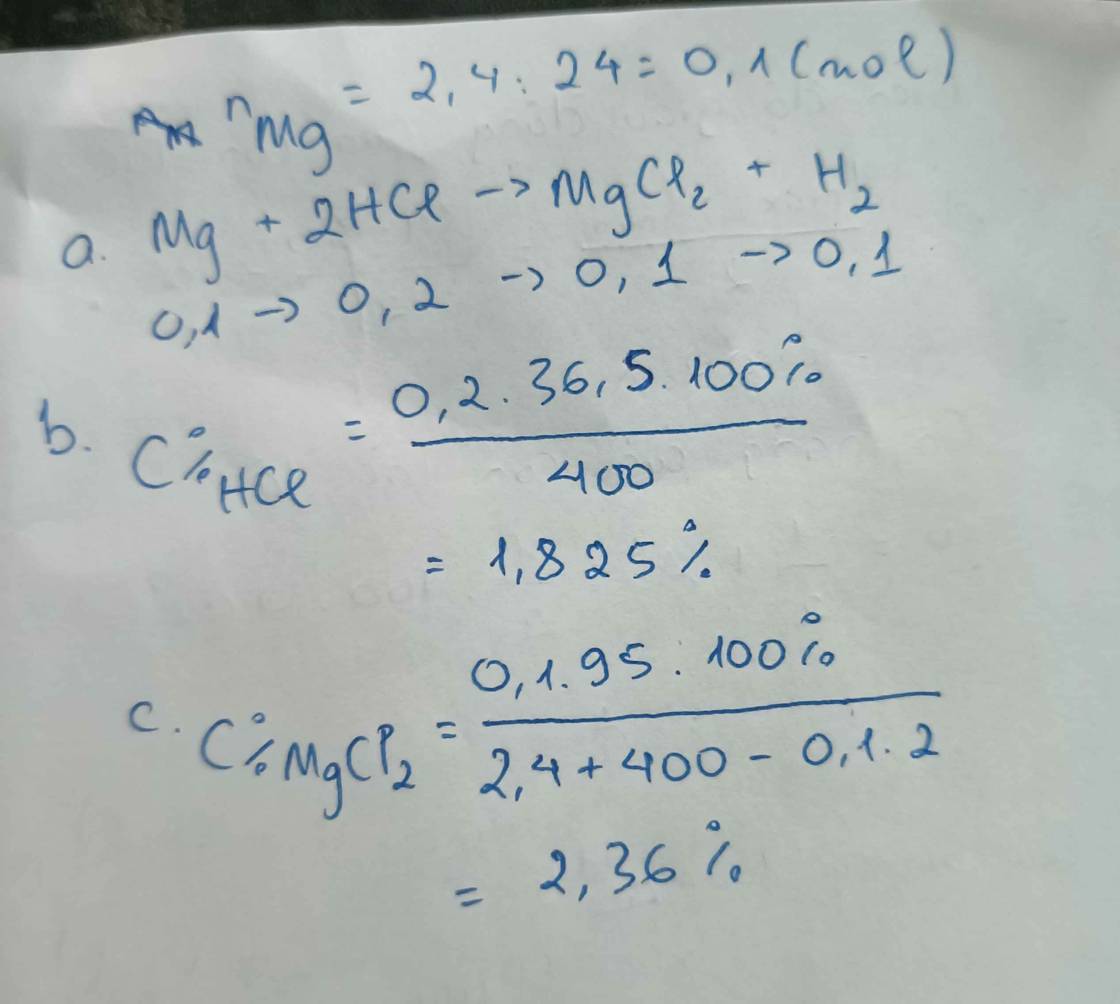
\(n_{Zn}=\dfrac{13}{65}=0,2(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{HCl}=0,4(mol)\\ \Rightarrow C\%_{HCl}=\dfrac{0,4.36,5}{100}.100\%=14,6\%\\ c,n_{ZnCl_2}=n_{H_2}=0,2(mol)\\ \Rightarrow m_{ZnCl_2}=0,2.136=27,2(g)\\ \Rightarrow C\%_{ZnCl_2}=\dfrac{27,2}{13+100-0,2.2}.100\%\approx 24,16\%\)
Ủa thịnh THCS HTA đúng kh? Này đề thi giữa kì hóa mà thịnh đi hỏi hả ;) tui méc thầy nha