Hòa tan m gam Mg trong 500ml dung dịch chứa hỗn hợp H2SO4 0,4M và Cu(NO3)2 đến phản ứng hoàn toàn thu được dung dịch X; 2 gam hỗn hợp kim loại và hỗn hợp khí X gồm 0,03 mol H2 và 0,02 mol N2. Giá trị của m là
A. 5,08. .
B. 3,52.
C. 3,12.
D. 4,64
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : C
Xét 0,05 mol X : Áp dụng qui tắc đường chéo : nN2 = 0,02 mol ; nH2 = 0,03 mol
=> Giả sử phản ứng tạo NH4+ : x mol
=> nH+ = 12nN2 + 2nH2 + 10nNH4+
=> x = 0,01 mol
Do khí có H2 => NO3- phải hết trước H+
Sau phản ứng có hỗn hợp kim loại => Cu2+ ; H+ phản ứng hết
=> Trong dung dịch chỉ còn lại : NH4+ ; SO42- ; Mg2+
=> BT điện tích : nMg2+ = 0,195 mol
BT Nito : nNO3 = nN2.2 + nNH4+ = 0,05 mol => nCu2+ = 0,025 mol = nCu
=> mMg dư = 2 – 0,025.64 = 0,4g
=> m = mMg dư + 24. nMg pứ = mMg dư + 24nMg2+ ( dd) = 5,08g

Đáp án C
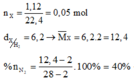
![]()
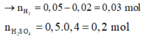
Vì sau phản ứng thu được hỗn hợp kim loại →H+ hết
Mg → Mg2+ + 2e
12H+ + 2NO−3 +10e → N2 + 6H2O
0,24 ← 0,04 ← 0,2 ← 0,02 mol
2H+ + 2e → H2
0,06 ← 0,06 ← 0,03
Cu2+ + 2e → Cu
![]()
=> Sản phẩm có NH4NO3
n H + c ò n l ạ i = 0,4 - 0,3 = 0,1 mol
10H+ + NO−3 + 8e → NH+4 + 3H2O
0,1 → 0,01 → 0,08 mol
![]()
![]()
![]()
m M g p h ả n ứ n g = 0 , 195 . 24 = 4 , 68 g
=> m = 0,4 + 4,68 = 5,08 g

Đáp án C

12H+ + 2NO−3 + 10e → N2 +6H2O
0,24 ← 0,04 ← 0,2 ← 0,02 mol
2H+ + 2e → H2
0,06 ← 0,06 ← 0,03
Cu2+ + 2e → Cu
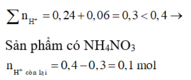
10H+ + NO−3 + 8e → NH+4 + 3H2O
0,1 → 0,01 → 0,08 mol
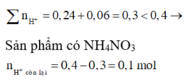
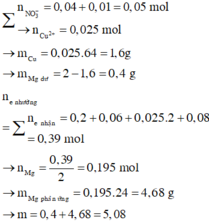
Đáp án A
Khí X có chứa H2 à dung dịch X không có muố nitrat;
Sau phản ứng thu được hỗn hợp kim loại à Mg dư à H+ đã phản ứng hết
Số mol H+ phản ứng = 0,4 (mol); Số mol H+ tạo ra H2 và N2 = 0,3 à có muối amoni trong dung dịch X
Số mol NH4+ = 0 , 4 - 0 , 3 10 = 0 , 01 (mol)à Số mol Cu(NO3)2 (bđ) = 0,025 (mol)
Theo bảo toàn e à số mol Mg phản ứng = 0,195 (mol); khố lượng Mg dư = 0,4 gam
à Khối lượng Mg (ban đầu) = 5,08 gam