Hoà tan hết 2,16 gam FeO trong 0,1 mol HNO3 vừa đủ thấy thoát ra khí X là sản phẩm khử duy nhất. Xác định X.
A. NO2
B. N2
C. N2O
D. NO
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có nFeO=0,03 mol= nFe(NO3)3
Bảo toàn nguyên tố N:
nN (HNO3)= nN (Fe(NO3)3)+ nN (khí X)→ 0,1=0,03.3+ nN(khí X)
→ nN(khí X)= 0,01 mol
QT cho e:
Fe+2→ Fe+3+ 1e
0,03 0,03 mol
Quá trình nhận e:
-Nếu khí có 1 nguyên tử N: Gọi a là số oxi hóa của N có trong khí X
N+5 + (5-a) e→ N+a
(5-a).0,01 0,01
Theo ĐL bảo toàn electron có: 0,03= 0,01(5-a) → a= +2 → X là khí NO
-Nếu khí X có 2 nguyên tử N: → nKhí= nN(khí)/2= 0,005 mol
2N+5 + 2(5-a) e→ N2+a
(5-a).0,01 0,005
Theo ĐL bảo toàn electron có: 0, 03= 0,01.(5-a) → a= +2→LOại
Vậy X là NO
Đáp án D

Định hướng tư duy giải
Ta có:
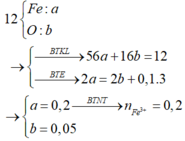
Cho Fe vào dung dịch X sẽ có NO (c mol) bay ra :
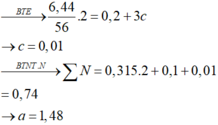

Quy hỗn hợp A gồm (FeO, Fe3O4, Fe2O3) thành hỗn hợp (FeO, Fe2O3)
Ta có các phản ứng:
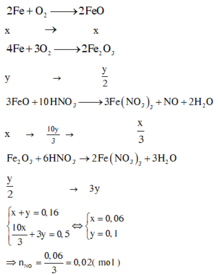
Đáp án D

Đáp án : C
Bảo toàn e :
3nAl + 2nMg= 2 n S O 2 + 3 n N O + n N O 2 + 8 n N 2 O = 1,4 mol
Và 27nAl + 24nMg = 15g
=> nAl = 0,2 mol
=> %mAl = 36%
nFeO = 0,03; Bảo toàn nguyên tố Fe ⇒ nFe(NO3)3 = 0,03
Bảo toàn nguyên tố N: nN/khí = nHNO3 – 3nFe(NO3)3 = 0,1 – 0,03.3 = 0,01
Nhận e:
N+5 + k(e) → Nx
0,01k ← 0,01 (mol)
Cho e:
Fe2+ → Fe3+ + 1e
0,03 → 0,03 (mol)
Áp dụng định luật bảo toàn e có: 0,01k = 0,03 ⇒ k =3
k =3 ⇒ x= 2 ⇒ Khí đó là NO
Đáp án D.