Cho 1,12 gam bột Fe và 0,24 gam bột Mg tác dụng với 250 ml dung dịch CuSO 4 , khuấy nhẹ cho đến hết màu xanh, nhận thấy khối lượng kim loại sau phản ứng là 1,76 gam. Nồng độ đung dịch CuSO 4 trước phản ứng là
A. 0,01 M
B. 0,02M
C, 0,03M
D. 0,04M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Khối lượng kim loại tăng: 1,88 – (1,12 + 0,24) = 0,52 (gam)
Trước hết, Mg tác dụng với CuSO4
Mg + CuSO4 → MgSO4 + Cu (1)
nMg = 0,1 mol ⇒ nCuSO4 =0,1 mol
Từ (1) ⇒ 0,1 mol Mg tác dụng với 0,1 mol CuSO4 sinh ra 0,01 mol Cu đã làm cho khối lượng kim loại tăng:
0,01.(64 – 24) = 0,4 (gam)
⇒Phản ứng giữa Fe và CuSO4 làm cho khối lượng kim loại tăng:
0,52 – 0,4 =0,12 g
Fe + CuSO4 → FeSO4 + Cu (2)
![]()
Vậy:


Đáp án C
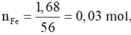
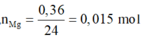
Nếu Fe và Mg phản ứng hết:
![]()
=> mCu = 64.0,045 = 2,88 g > 2,82 g
=> Chứng tò Fe phản ứng còn dư.
![]()
![]()
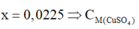
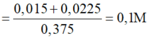

Đáp án A
Phương trình hóa học:
Mg + CuSO4 → MgSO4 + Cu (1)
Fe + CuSO4 → FeSO4 + Cu (2)
Có: nMg = 0,01 mol và nFe = 0,02 mol
Theo (1) và (2), nếu Mg và Fe phản ứng hết thì thu được 0,03 mol Cu.
Khối lượng kim loại thu được sau phản ứng là:
0,03 .64 = 1,92 (gam)
Thực tế chỉ thu được 1,88 gam kim loại. Chứng tỏ kim loại đã cho không phản ứng hết.
Mg có tính khử mạnh hơn Fe nên phản ứng trước.
Lượng Cu sinh ra ở (1) là 0,01 mol tương ứng với khối lượng 0,64 (gam)
Khối lượng Fe dư và Cu sinh ra ở (2) là: 1,88 – 0,64 = 1,24 (gam)
Đặt khối lượng Fe tham gia ở (2) là x, khối lượng sắt dư là (1,12 – 56x) và khối lượng Cu sinh ra ở (2) là 64x.
Ta có: (1,12-56x) + 64x = 1,24 => x = 0,015
Lượng CuSO4 trong 250 ml dung dịch đã phản ứng hết:
0,015 + 0,01 = 0,025(mol)
Nồng độ mol của dung dịch đã dùng là : 0,025/0,25 = 0,1mol/l

Khối lượng kim loại tăng là : 1,88 - 1,12 - 0,24 = 0,52 (g)
Mg là kim loại mạnh hơn Fe nên Mg phản ứng trước.
Mg + CuSO4 → MgSO4 + Cu (1)
0,01 → 0,01 (mol)
Mg phản ứng hết làm khối lượng tăng là :
64 . 0,01 - 24 . 0,01 = 0,40 (g)
Phản ứng của Fe làm khối lượng tăng thêm là : 0,52 - 0,40 = 0,12(g)
Fe + CuSO4 → FeSO4 + Cu (2)
Theo (2), ta có:
1 mol CuSO4 phản ứng làm khối lượng tăng 64 - 56 = 8 (g)
x mol <-------------------------------------------------- 0,12 g
x=0,128=0,015(mol)x=0,128=0,015(mol)
Số mol Fe ban đầu là 1,1256=0,02(mol)>0,0151,1256=0,02(mol)>0,015
Vậy Fe còn dư và CuSO4 hết.
Nồng đô mol của CuSO4 là : (0,01+0,015).1000250=0,1M(0,01+0,015).1000250=0,1M.
Đáp án D
Nhận xét: khi cho bột kim loại vào dung dịch, khối lượng kim loại sau phản ứng sẽ tăng lên.
Ta có khoảng sau: