Dung dịch X gồm các cation Ca2+; Mg2+; Ba2+ và anion Cl-; (các anion có số mol bằng nhau). Để kết tủa hết các cation trong X cần dùng vừa đủ 30 ml K2CO3 2M và lượng kết tủa thu được nặng 6,49 gam. Mặt khác, đem cô cạn X rồi nung nóng trong không khí đến khối lượng không đổi thì thu được m gam chất rắn khan. Giá trị của m là:
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

9 tháng 1 2019
Đáp án : D
ta có : nCO3 = nCation trong A = ½ nAnion trong A ( bảo toàn điện tích )
=> nAnion trong A = 0,5 mol

3 tháng 7 2018
Đáp án B
Ca2++ CO32-→ CaCO3
Mg2+ + CO32-→ MgCO3
Ba2+ + CO32-→ BaCO3
2H++ CO32-→ CO2+ H2O
Số cation còn lại trong dung dịch là Na+ và K+

9 tháng 11 2017
Chọn D vì
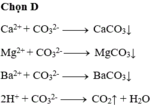
Ca2+ + CO32- → CaCO3↓
Mg2+ + CO32- → MgCO3↓
Ba2+ + CO32- → BaCO3↓
2H+ + CO32- → CO2↑ + H2O
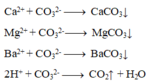

Đáp án A
Khi cho dung dịch K2CO3 vào dung dịch X thì có các phản ứng:
Áp dụng định luật bảo toàn điện tích cho dung dịch X ta có:
Khi đun nóng dung dịch X rồi nung trong không khí đến khối lượng không đổi thì có các phản ứng:
Với M là công thức chung của Ca, Mg và Ba.
Do đó chất rắn khan thu được cuối cùng chứa Ca2+, Mg2+, Ba2+, Cl-, O2- (trong oxit) với